
科目:初中化学 来源:轻巧夺冠人教版九年级化学下 题型:043
钛
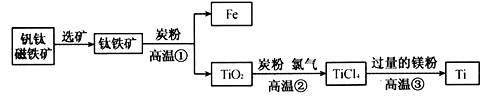
(Ti)因为具有神奇的性能越来越引起人们的关注,常温下钛不和非金属、强酸反应,红热时却能与常见的非金属单质反应.钛是航空、军工、电力等方面的必需原料.目前大规模生产钛的方法是:第一步,金红石
(主要成分TiO2)、炭粉混合在高温条件下通入氯气制得TiCl4和一种可燃性气体.该反应的化学方程式________________.该反应的还原剂是________________.第二步,在氩气的气氛中,用过量的镁在加热条件下与
TiCl4反应制得金属钛.该反应的化学方程式为________________.简述从上述所得产物中获得纯净的金属钛的步骤和相关的化学方程式.
________________________________________.
查看答案和解析>>
科目:初中化学 来源:化学课外练习第2册九年级下学期用 北京课改版 题型:022
| |||||||||||||||
查看答案和解析>>
科目:初中化学 来源: 题型:058
钛
(Ti)因为具有许多神奇的性能而越来越引起人们的关注,常温下钛不和非金属、强酸反应;红热时,却可与许多常见的非金属单质反应,钛是航空、宇航、军工、电力等方面的必需原料,地壳中含钛矿石之一称金红石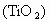 ,目前大规模生产钛的方法是:
,目前大规模生产钛的方法是:
第一步:金红石、炭粉混合在高温条件下通入氯气制得
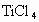 和一种可燃性气体,该步发生反应的化学方程式是_________________,该反应的还原剂是_______________.
和一种可燃性气体,该步发生反应的化学方程式是_________________,该反应的还原剂是_______________.
第二步:在氩气的气氛中,用过量的镁在加热条件下与
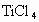 反应制得金属钛.
反应制得金属钛.
(1)
此反应的化学方程式是______________________;(2)如何由上述所得产物中获得纯净金属钛?简述主要实验步骤,并写出有关反应的化学方程式______________________.查看答案和解析>>
科目:初中化学 来源:江苏模拟题 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com