
【题目】化学是一门以实验为基础的学科,请结合下列实验装置回答问题
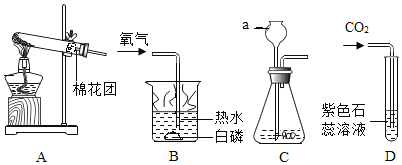
(1)写出图中所示实验仪器的名称:a_____;
(2)写出A装置用高锰酸钾制取氧气的化学方程式_____。
(3)连接A、B装置,观察到B装置热水中的白磷燃烧,说明燃烧需要_____
(4)利用C、D装置制取CO2.C中发生的化学反应方程式为_____;D中观察到的实验现象为_____
【答案】长颈漏斗 2KMnO4![]() K2MnO4+MnO2+O2↑ 氧气 CaCO3+2HCl=CaCl2+H2O+CO2↑ 紫色的石蕊试液变红色
K2MnO4+MnO2+O2↑ 氧气 CaCO3+2HCl=CaCl2+H2O+CO2↑ 紫色的石蕊试液变红色
【解析】
解:(1)据图可知仪器a是长颈漏斗;
(2)高锰酸钾在加热的条件下分解为锰酸钾、二氧化锰和氧气;化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3)将生成的氧气通入热水中的白磷附近发现热水中的白磷发生了燃烧,这一现象说明了燃烧需要氧气;
(4)实验室中制取二氧化碳的原理是碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,化学反应方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳与水反应生成碳酸,碳酸能使紫色的石蕊试液变红色。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】下列关于C+O2![]() CO2的说法不正确的是( )
CO2的说法不正确的是( )
A. 表示碳与氧气在点燃条件下反应生成二氧化碳
B. 参加反应的氧气与生成的二氧化碳的分子个数比为1:1
C. 反应前后碳原子和氧原子的个数均不变
D. 6g的碳在20g氧气中完全燃烧生成二氧化碳的质量为26g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图表示初中化学里常见物质之间的转化关系(部分生成物未全部标出),A、B为常见的气体,C为常见液体,F是一种具有刺激性气味的气体,其水溶液呈碱性,甲是一种常见建筑材料的主要成分,乙为植物光合作用必需的物质,丙和戊均为黑色固体,已为紫红色金属。
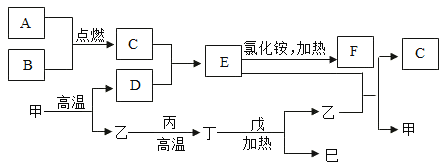
(1)写出C、甲、乙的化学式:C_____;甲_____;乙_____。
(2)写出E和乙反应的化学方程式_____。
(3)将10g甲高温煅烧一段时间,冷却后投入足量的稀盐酸中充分反应,下列有关该变化过程的说法中,不正确的是_____(填字母)
A煅烧后固体中氧元素的质量分数减小
B煅烧越充分,消耗的盐酸越少
C共生成11.1g氯化钙
D共生成4.4g二氧化碳
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列4个图像中,能正确反映对应变化关系的是
|
|
|
|
A向一定量的硝酸银溶液中插入铜丝 | B向一定量的饱和石灰水中加入氧化钙 | C将水通电电解一段时间 | D两份等体积的5%过氧化氢溶液,向其中一份加入少量MnO2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙为初中常见物质,其转化关系如下图(“→”表示由一种物质转化成另一种物质,反应条件、部分反应物和生成物已略去)。
![]()
(1)若甲,乙、丙均含有同一种金属元素,人体缺少它会贫血,甲为单质,乙含有两种元素,丙含有三种元素,则丙可能是_____。
(2)若甲、乙、丙均为含有钙元素的化合物,甲与水反应生成乙并放出大量的热。甲的俗称是_____。则甲→乙的化学方程式为_____,丙可能是_____(写一种)。
(3)若甲、乙、丙为氧化物,除氧元素外另一种元素均不相同,且三种物质常温下依次为固态、气态和液态,则甲可能是_____(写一种)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.等质量和等质量分数的氢氧化钠和硫酸溶液,充分混合后,加入氯化铁溶液后产生红褐色沉淀
B.等质量的甲烷和一氧化碳充分燃烧,一氧化碳消耗的氧质量大
C.氧化铁和氧化亚铁中铁元素含量相等,则两种物质中氧元素的质量比为2:3
D.将一定质量的高锰酸钾加热一段时间后,试管中锰元素和氧元素质量比可能为11:12
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用实验现象推断物质是常用的实验手段
(1)联欢会上,小欢表演了一个化学魔术﹣﹣变色纸花。她向白色小花A、紫色小花B、红色小花C上分别喷洒无色的M溶液,三朵纸花分别变成了红色、蓝色和紫色。则溶液M可能是:_____(填化学式)。
(2)小花查阅资料得知,牵牛花所含花青素与紫色石蕊具有相似的性质。将一朵紫色的牵牛花浸泡在肥皂水里,牵牛花很快变蓝,将另一朵牵牛花浸泡在家庭厨房里的某种常用调味品中,牵牛花变成了红色,根据上述现象回答:
①肥皂水的pH_____7(填“>”“=”或“<”)。
②小红选用的调味品可能是_____(填名称)。
(3)一包白色粉末可能由硫酸钠、碳酸钠、氯化钡、硫酸铜、氢氧化钠、氯化钠中的一种或几种组成。小刚为了测定该白色粉末的组成,设计了如下实验。
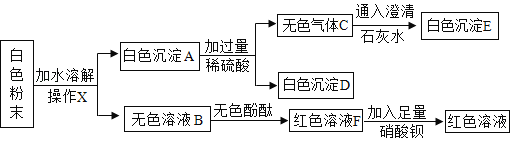
请根据如图实验现象帮助小刚判断:
①操作X为_____。
②白色粉末中可能含有的物质是_____。
③写出C→E的化学方程式_____。
④向红色溶液F中加入足量硝酸钡的目的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上常用电解饱和食盐水的方法制取烧碱,某化学兴趣小组为了探究久置的工业烧碱的成分,进行了如下实验:
(1)取少量样品于烧杯中,向其中加入过量稀盐酸,观察到有气泡产生,说明样品中含有_________,接着又向烧杯中继续加入硝酸银溶液,出现了白色沉淀(已知氯化银是白色沉淀),得出结论:样品中____________(填“一定”或“不一定”)含有氯化钠。
(2)丙同学认为除了需要确认是否含有氯化钠外,还需要确认样品中是否含有氢氧化钠,于是,大家又进行了以下实验:
①另取少量样品溶解于水,向其中加入过量硝酸钙溶液,产生白色沉淀,然后过滤、洗涤;
②取少量滤液滴入酚酞,溶液变红;
③向滤液中加入足量稀硝酸,再滴入硝酸银溶液后产生白色沉淀;
由此判断,实验中滤渣的成分是_________(填化学式)。
(3)根据以上实验,得出的结论正确的是________(填序号)。
A、样品中无NaCl
B、样品中只有NaOH和Na2CO3
C、样品中无NaOH
D、样品中有Na2CO3、NaOH和NaCl
(4)配制100mL质量分数10%的氢氧化钠溶液(密度1.11g/mL),需要质量分数40%的氢氧化钠溶液(1.43g/mL)_________mL,水________mL。(计算结果精确到0.1)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com