
【题目】如图所示为实验室常用的制气装置,据此回答下列问题。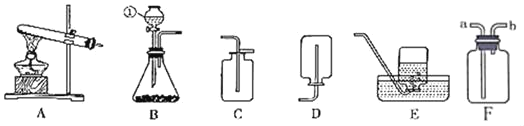
(1)写出仪器①的名称:_____。
(2)实验室用高锰酸钾制氧气,发生装置选_____(填字母),收集装置选_____(填字母),反应的化学方程式为_____。
(3)实验室常用锌和稀硫酸混合制取氢气,发生装置选_____(填字母)。收集氢气常用D或E装置,说明氢气具有_____的性质(写出1条即可)。
(4)实验室也能用F装置收集CO2气体,若要检验CO2气体是否收集满,可以将燃着的木条放在_____(填“a”或“b”)导管口。
【答案】分液漏斗 A C或E 2KMnO4![]() K2MnO4+MnO2+O2↑ B 氢气难溶于水或氢气的密度比空气小 b
K2MnO4+MnO2+O2↑ B 氢气难溶于水或氢气的密度比空气小 b
【解析】
(1)仪器①的名称是分液漏斗。
故填:分液漏斗。
(2)实验室用高锰酸钾制氧气需要加热,发生装置选A;
因为氧气的密度比空气大,可以用向上排空气法收集,即用C装置收集,氧气不易溶于水,可以用排水法收集,即用E装置收集;
反应的化学方程式为:2KMnO4 ![]() K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。
故填:A;C或E;2KMnO4 ![]() K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。
(3)实验室用锌和稀硫酸混合制取氢气不需要加热,发生装置选B;
收集氢气常用D或E装置,说明氢气具有密度比空气小、不溶于水。
故填:B;密度比空气小或不溶于水。
(4)实验室也能用F装置收集CO2气体,若要检验CO2气体是否收集满,由于二氧化碳密度比空气大,可以将燃着的木条放在b导管口。
故填:b。


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:初中化学 来源: 题型:
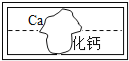
【题目】在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.
探究一 M溶液中的溶质是什么?
(1)(提出猜想)该组同学认为M溶液的溶质有两种可能:①是 ,②是CaCl2.
(收集资料)CaCl2水溶液呈中性.
(2)(设计实验)同学们设计了如下方案并进行实验:
实验操作 | 实验现象 | 实验结论 |
取少量M溶液于试管中,向其中滴加 | | 猜想①正确,碳酸钠与其反应的化学方程式为 |
探究二 过滤后澄清滤液中会有哪些溶质?
(提出猜想)猜想一:NaOH和Na2CO3;猜想二:_____;猜想三:NaOH
(3)(实验验证)同学们针对“猜想一”进行了如下实验:
实验步骤 | 实验现象 | 实验结论 |
取样于试管中,滴入几滴稀盐酸 | 没有气体产生 | “猜想一”不成立 |
他们的实验结论是否正确? ,理由是 .
(4)(继续探究)设计实验方案确定滤液中溶质的组成.
实验操作 | 实验现象 | 实验结论 |
分别取少量滤液于A、B两支试管中,A中加入CaCI2溶液,B中加入 溶液 | 若A中产生白色沉淀,B中没有沉淀 | “猜想一”成立 |
| “猜想二”成立 | |
| “猜想三”成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】单质及化合物是中学化学学习和研究的重要内容。
(1)如图为钠的原子结构示意图。下列说法不正确的是_________。

A X=1 B 钠原子的中子数为11
C 钠离子的符号为Na D 钠元素位于元素周期表中第三周期
(2)如图所示,用“W”型玻璃管进行微型实验。

①b处发生的现象是_____________;②写出a处发生反应的化学方程式___________;③写出为a处发生反应提供热量的化学反应方程式________
(3)浓硫酸和浓盐酸敞口放置均会变稀的原因________?
(4)已知:2Na2O2+2H2O=4NaOH+O2↑;2Na2O2+2CO2=2Na2CO3+O2↑。实验室敞口放置的过氧化钠(Na2O2)已部分变质,取少量该固体样品于试管中,加足量水,可观察到什么现象________?如何检验验证该水溶液中含有的两种溶质________。(简要写出实验步骤及现象)
(5)某同学为了测定氢氧化钠变质情况,取该样品固体20g,向其中加入足量的水,充分溶解;再加入足量的氯化钡溶液,充分反应后,过滤、洗涤、烘干,称得沉淀的质量为19.7g。计算该样品中氢氧化钠的质量分数________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是A、B、C三种固体物质的溶解度曲线
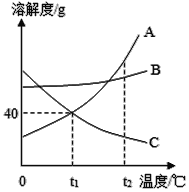
(1)t2℃时,A、B、C三种物质的溶解度由大到小的顺序是_____
(2)将等质量的A、C两种物质分别配成t2℃时的饱和溶液,所需溶剂的质量较多的是_____
(3)t1℃时,将40gA和40gB分别加入到盛有100g水的烧杯中,达到饱和状态的是_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下列实验装置图回答问题.
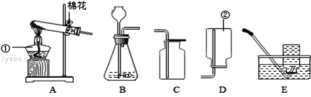
(1)写出仪器①、②的名称:①______、②______.
(2)若用高锰酸钾制取并收集O2,可选用的装置组合为______(选填字母),该反应的化学方程式为__________________。
(3)实验室用B装置制取CO2的化学方程式为________________________。若用C装置收集CO2,则检验收集满CO2,则检验收集满CO2的方法是_______________。
(4)按照下图把收集好的CO2依次通入盛有石蕊试液、澄清石灰水和高低蜡烛的试管或烧杯中,F中可以观察到得现象是___________________________________,G中发生的化学反应方程式为________________________。写出H中的可以观察到的现象是____________________。

(5)天然气是一种重要的化石燃料,它的主要成分是甲烷,甲烷是结构最简单的有机化合物.在通常情况下,甲烷是一种无色、无味、密度比空气小的气体,难溶于水。利用图J收集甲烷,请补充画好J图中的导管。_____。
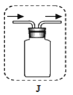
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在合成氨工业中,常用碳酸钾溶液吸收产生的二氧化碳得到碳酸氢钾,反应的化学方程式为:K2CO3+CO2+H2O=2KHCO3。现向碳酸钾溶液中通入二氧化碳,恰好完全反应,得到溶质质量分数为10%的溶液50 g。试计算:
(1)若把该50 g溶液稀释成溶质质量分数为4%的溶液,需加水的质量是___g。
(2)原碳酸钾溶液中溶质的质量分数(结果精确到0.1%)。________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某班同学用氢氧化钠溶液和稀盐酸进行中和反应实验:
(1)甲同学实验操作如下:
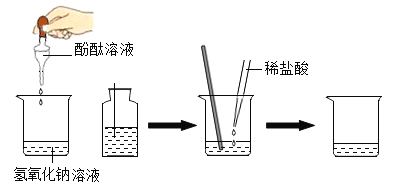
在烧杯中加入约5 mL氢氧化钠溶液、滴入几滴无色酚酞溶液,此时溶液呈________色。接着用滴管滴入一定量的稀盐酸,再用玻璃棒____________,发现溶液为无色,于是甲同学得出两者恰好中和的结论,反应的化学方程式为________________________。
(2)乙同学对甲同学的结论提出了质疑,并对反应后溶液中的溶质成分进行探究。
(实验探究)反应后溶液中的溶质是什么?
猜想一:只有NaCl
猜想二:NaCl和HCl
猜想三:NaCl和NaOH
以上猜想中,你觉得不合理的是________________。
为了验证另外两种猜想,乙同学设计如下实验方案。
实验操作 | 实验现象 | 实验结论 |
取少量反应后的溶液于试管中滴入Na2CO3溶液 | ________ | 猜想二成立 |
(反思交流)实验结束后,废液处理方法正确的是______(填序号)。
A 倒入下水道 B 倒入废液缸 C 带出实验室
(拓展延伸)乙同学再设计一个验证猜想二的实验:取少量反应后的溶液于试管中加入少量氧化铜粉末,若________________________,猜想二成立。
(3)用溶质质量分数为5%的NaOH溶液完全中和73 g10%的稀盐酸,需NaOH溶液多少克________?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质甲、乙、丙的溶解度曲线如图所示。下列说法错误的是
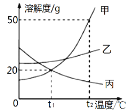
A. t1℃时,甲、丙饱和溶液的溶质质量分数都是16.7%
B. 使甲从溶液中结晶,只能用冷却热饱和溶液的方法
C. t2℃时150 g甲的饱和溶液降温到t1℃,能析出30g晶体
D. 将t2℃的三种物质饱和溶液分别降温到t1℃,所得溶液的溶质质量分数大小关系是乙>甲>丙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校的学习小组根据下面给出实验装置(另有托盘天平可用),粗略测定铜锌合金(黄铜)中锌的质量分数(黄铜已加工成粉末)。
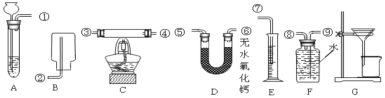
(分析思考)
同学们通过充分“交流-分析-讨论”后一致认为,设计以下三种实验方案均可测出黄铜中锌的质量分数。同学们用过量稀硫酸与称取的 a克黄铜粉样品进行充分反应后,实验中测定了以下数据:
①测定生成H2的体积b升(已知氢气的密度为ρ)。
②过滤、洗涤、烘干后,测定漏斗中剩余固体的纯净质量为c克。
③充分反应后,测定 A 装置中仪器和药品总质量减少了d克。
(方案一)小悦仅选用一个实验装置 A 进行实验,并用测定的数据,通过计算,求出黄铜中锌的质量分数为____。
(方案二)小华选用两个装置__(填装置编号)进行实验,并用数据__(填数据编号),通过计算也求出了黄铜中锌的质量分数。
(方案三)小琳选用三个实验装置进行实验,装置连接的顺序是(用装置接口处的编号表示)__,并用测定的数据,通过计算也求出了黄铜中锌的质量分数。
(反思评价)小组对上述三种实验方案进行了综合评价,认为方案___最简单易行。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com