
| Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀的pH | 1.9 | 4.7 |
| 沉淀完全的pH | 3.2 | 6.7 |
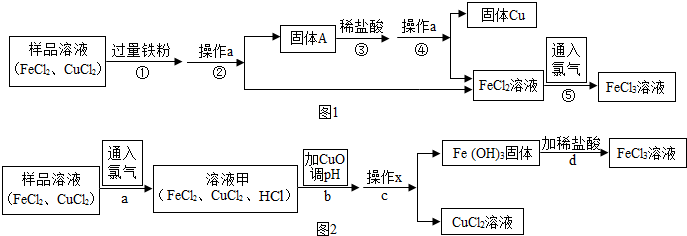
分析 (1)铁和氯化铜反应生成氯化亚铁和铜;
铁和稀盐酸反应生成氯化亚铁和氢气;
过滤能够把不溶于水的固体从液体中分离出来;
(3)氧化铜和稀盐酸反应生成氯化铜和水;
(4)加入稀硝酸时,会带入硝酸根离子,加入稀硫酸时,会带入硫酸根离子,加入稀醋酸时,会带入醋酸根离子.
解答 解:(1)①中铁和氯化铜反应生成氯化亚铁和铜,发生的化学方程式为:Fe+CuCl2═FeCl2+Cu,属于置换反应.
故填:Fe+CuCl2═FeCl2+Cu;置换反应.
(2)步骤②中的操作a名称是过滤;
步骤③中加入稀盐酸的目的是除去过量的铁粉.
故填:过滤;除去过量的铁粉.
(3)盐酸与氧化铜反应的化学方程式为:CuO+2HCl=CuCl2+H2O;
步骤b调节溶液的pH到3.2~4.7时,铁离子能够以氢氧化铁的形式全部沉淀出来,而铜离子不能形成沉淀.
故填:CuO+2HCl=CuCl2+H2O;3.2~4.7.
(4)加入稀硝酸时,会带入硝酸根离子,加入稀硫酸时,会带入硫酸根离子,加入稀醋酸时,会带入醋酸根离子,因此在保存FeCl3溶液时,常向FeCl3溶液中加入稀盐酸.
故填:C.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | NB | B. | BN | C. | bN | D. | B3N3 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 物 质 | Cu(OH)2 | Fe (OH)3 |
| 开始沉淀pH | 4.2 | 1.2 |
| 完全沉淀pH | 6.7 | 3.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 10 ml的量筒 | B. | 100 ml的量筒 | ||
| C. | 50 ml的量筒和胶头滴管 | D. | 500 ml的量筒和胶头滴管 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com