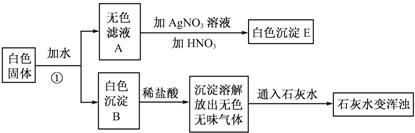
(2010?泉州)上完体育课后,小强同学往一瓶矿泉水中加入一片“泡腾片”(其商标部分内容如图所示).立即产生大量气泡,片刻成为一瓶可口的饮料,这引起了身边同学 极大兴趣,于是大家决定对其进行如下的探究:

探究活动一:泡腾片的发泡原理
【查阅资料】碳酸氢钠(NaHCO
3)俗称“小苏打”与酸反应会生成二氧化碳;柠檬酸是一种酸.
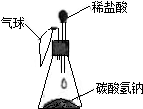
【进行实验】按如图装置进行实验:
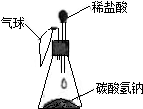
当观察到
产生大量气泡,气球胀大
产生大量气泡,气球胀大
时,说明碳酸氢钠会与稀盐酸反应.联想到已学过的化学反应Na
2CO
3+2HCl=2NaCl+H
2O+CO
2试写出碳酸氢钠与稀盐酸反应的化学方程式:
NaHCO3+HCl=NaCl+H2O+CO2↑
NaHCO3+HCl=NaCl+H2O+CO2↑
.
【结论】由实验可知:泡腾片放入水中的发泡原理是小苏打与配料中的
柠檬酸
柠檬酸
反应的结果.
探究活动二:NaHCO
3和Na
2CO
3的热稳定性
【提出问题】NaHCO
3和Na
2CO
3与盐酸反应都会生成CO
2,那么两者的热稳定性又如何?
【进行猜想】NaHCO
3和Na
2CO
3的热稳定性差,受热都会发生分解反应.
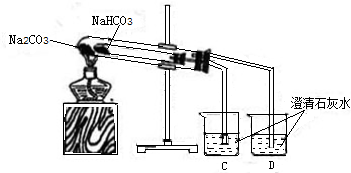
【设计并进行实验】为验证猜想,同学们设计了下图装置并进行实验:
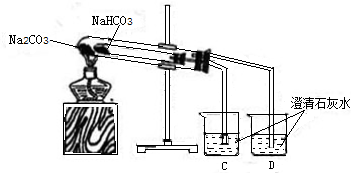
【实验现象】
①装有NaHCO
3的小试管内壁有水珠生成.
②烧杯C、D中导管口有气泡冒出,但是有烧杯C中澄清石灰水变浑浊.
③充分加热后,大试管中的固体无明显变化,小试管中仍有少量白色固体残留.
【实验结论】NaHCO
3受热会分解,生成水、
二氧化碳
二氧化碳
和一种白色固体,而Na
2CO
3受热不分解,因此,以上猜想
错误
错误
(选填“正确”或“错误”).写出烧杯C中澄清石灰水变浑浊的反应化学方程式:
Ca(OH)2+CO2═CaCO3↓+H2O
Ca(OH)2+CO2═CaCO3↓+H2O
.
【交流与讨论】根据反应物的组成元素,同学们认为残留的白色固体可能是Na
2CO
3或NaOH中的一种,为检验该白色固体,小强设计了如下方案:
Ⅰ.往残留固体中滴加稀盐酸,观察现象,判断白色固体是否为Na
2CO
3.
Ⅱ.将残留固体溶于水后,滴加无色酚酞试液,判断白色固体是否为NaOH.同学们经过讨论一致认为方案Ⅱ不行,理由是
碳酸钠和氢氧化钠的水溶液都呈碱性,都能使酚酞变红
碳酸钠和氢氧化钠的水溶液都呈碱性,都能使酚酞变红
.
小强通过方案Ⅰ的实验得出白色固体是Na
2CO
3,若让你用另一种试剂来验证Na
2CO
3,你会选用
Ca(OH)2
Ca(OH)2
试液.
【拓展与应用】
①Na
2CO
3固体混有少量NaHCO
3,可采用
C
C
(填序号)的方法除去.
A.加盐酸 B.通入CO
2 C.加热
②保存该泡腾片应注意
防潮防晒
防潮防晒
.