

分析 (1)根据锂元素原子的最外层电子数目的特点分析元素的性质;
(2)根据构成物质的粒子来分析;
(3)根据氯原子在化学反应中所起的作用以及物质的结构决定物质的性质来分析;
(4)从铁生锈的原理及食物变质的原因进行分析;
(5)根据溶解度曲线表示的意义进行分析解答.
解答 解:(1)锂原子最外层电子数为1,在化学反应中容易失去一个电子,带一个单位的正电荷,形成锂离子Li+;氢氧化锂与硫酸发生中和反应,反应的化学方程式为:2Li+H2SO4═Li2SO4+H2↑故填:失去;Li+;2Li+H2SO4=Li2SO4+H2↑;
(2)由题干信息可知,氟化钠是由氟离子和钠离子构成的;故填:离子;
(3)由题干信息可知,氯原子在化学变化中的种类和数目均没有改变,起到了催化作用;O3和O2的分子结构不同,所以化学性质也不同;故填:催化;分子结构不同;
(4)铁与氧气、水反应生成氢氧化铁的原理,吸收包装袋中的氧气和水分,从而延长食品的保质期;故填:bc;
(5)根据氯化钠和硝酸钾溶解度曲线可知,氯化钠的溶解度受温度影响较小,而硝酸钾的溶解度受温度影响较大,所以要从硝酸钾溶液中出硝酸钾结晶析出可采用降温结晶的方法;
其相同点是:都是易溶于水的物质;溶解度随温度变化的方向相同;两种物质在23℃时的溶解度相同;由于硝酸钾的溶解度受温度的变化影响很大,而氯化钠的溶解度受温度的影响较小,所以其不同点是:溶解度受温度影响的程度不一样;20℃时的饱和溶液溶质质量分数不相同;40℃100g饱和溶液降温到20℃析出晶体的质量不一样;故答案为:降温结晶;ABE.
点评 本题难度不大,考查的知识点较多,掌握钢铁生锈的原理、物质的结构、元素周期表的信息、溶解度曲线表示的意义等是正确解答本题的关键.


科目:初中化学 来源: 题型:选择题
| A. | 氧气常用于炼钢、潜水、急救等 | |
| B. | 称有气体可用于闪光灯、霓虹灯等 | |
| C. | 氮气常用做食品保护气 | |
| D. | 空气中二氧化碳的存在危害人类生存 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碱:火碱、纯碱、消石灰 | B. | 微量元素:钙、铁、锌、硒 | ||
| C. | 合成材料:铝合金、塑料、尼龙 | D. | 有机物:甲烷、乙醇、葡萄糖 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 归类 |
| A | 白酒、糖水、食盐水 | 常见溶液 |
| B | 蛋白质、油脂、维生素 | 营养物质 |
| C | 风能、氢能、太阳能 | 清洁能源 |
| D | 生铁、玻璃、玻璃钢 | 复合材料 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度/℃ | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
| 碳酸钠 | 12.2 | 21.8 | 39.7 | 53.2 | |

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
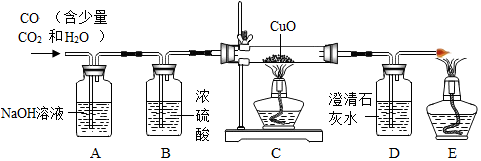
| 实验人员 | 红色固体(g) | 剩余红色固体(g) | 实验结论 |
| 甲 | 7.2 | 3.2 | 假设二成立 |
| 乙 | 4.08 | 2.48 | 假设三成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
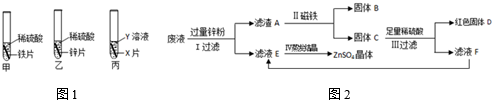
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com