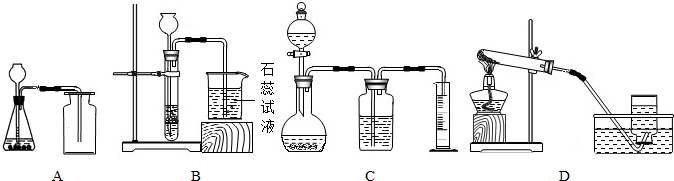
解:(1)用KMnO
4固体制取O
2,是固体的加热反应,所以我们可以用装置D作为实验装置;根据反应物是高锰酸钾、反应条件是加热写出化学反应式是:2KMnO
4 
K
2MnO
4+MnO
2+O
2↑;实验结束时,为防止水倒流入试管,引起试管炸裂,要先移出导管,再熄灭酒精灯.
故答案为:B、2KMnO
4 
K
2MnO
4+MnO
2+O
2↑、先把导气管移出水面,再熄灭酒精灯;
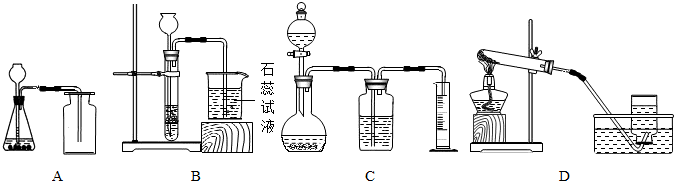
(2)装置A适合固体和液体在常温下反应,氧气和二氧化碳都可以在此装置中制取.过氧化氢溶液与二氧化锰固体反应制取氧气.大理石固体和稀盐酸液体反应制取二氧化碳气体.所以它制取的气体可能是CO
2或O
2;我们可以根据氧气支持燃烧,二氧化碳不支持燃烧的特点来检验是哪种气体,可用燃着的木条伸入集气瓶中,若木条熄灭为CO
2,若木条燃烧更旺为O
2.
故答案为:CO
2或O
2、用燃着的木条伸入集气瓶中,若木条熄灭为CO
2,若木条燃烧更旺为O
2;
(3)从图示可知,C装置的烧杯中盛放的是石蕊试液,它遇酸变红.二氧化碳不能直接使石蕊试液变红,所以a不合理;产生的CO
2与H
2O反应生成H
2CO
3,使紫色石蕊试液变红,是正确的;挥发出的氯化氢溶于水,使溶液呈酸性,使紫色石蕊试液变红,是正确的.
故选a;
(4)测量体积要用量筒,能测量体积的只有装置C;如果滴入的液体如果具有挥发性,就会混入生成的气体中,使得测量的值偏大.
故答案为:C、包含了滴入液体的体积.
分析:(1)用KMnO
4固体制取O
2,是固体的加热反应,据此选择实验发生装置;然后根据反应物是KMnO
4和反应条件是加热写出化学反应式;实验结束时,为防止水倒流入试管,要先移出导管,再熄灭酒精灯;
(2)装置A适合固体和液体在常温下反应,我们所了解的气体中的氧气和二氧化碳都可以在此装置中制取,据此写出可制取的气体;根据制取的气体的性质,选择验满的方法;
(3)先观察图形,可知B装置的烧杯中盛放的是石蕊试液,它遇酸变红.然后在选项abc中哪一个的解释不合理,就选哪一个.
(4)测量体积要用量筒;滴入的液体占有一定的体积,导致生成的气体体积偏大.
点评:发生装置的选择要考虑反应物的状态和反应条件,气体收集装置的选择要看收集气体的密度和溶水性,这些是化学实验中的常见问题,同学们一定要记清.

 K2MnO4+MnO2+O2↑;实验结束时,为防止水倒流入试管,引起试管炸裂,要先移出导管,再熄灭酒精灯.
K2MnO4+MnO2+O2↑;实验结束时,为防止水倒流入试管,引起试管炸裂,要先移出导管,再熄灭酒精灯. K2MnO4+MnO2+O2↑、先把导气管移出水面,再熄灭酒精灯;
K2MnO4+MnO2+O2↑、先把导气管移出水面,再熄灭酒精灯;

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案