
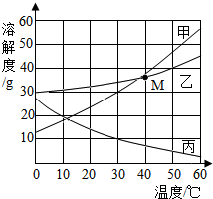
 甲、乙、丙三种物质的溶解度曲线如图所示.根据图中信息回答下列问题:
甲、乙、丙三种物质的溶解度曲线如图所示.根据图中信息回答下列问题:| 溶解度 |
| 溶解度+100g |


科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 完 |
| ? |
| 全 |
| ? |

查看答案和解析>>
科目:初中化学 来源: 题型:
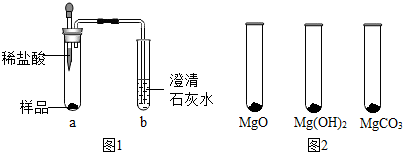 体操运动员在完成单杠、吊环项目时常用“镁粉”搓手,以起到防滑效果.某种“镁粉”中可能含有Mg、MgO、Mg(OH)2、MgCO3中的一种或两种固体,实验小组对其成分展开了探究.
体操运动员在完成单杠、吊环项目时常用“镁粉”搓手,以起到防滑效果.某种“镁粉”中可能含有Mg、MgO、Mg(OH)2、MgCO3中的一种或两种固体,实验小组对其成分展开了探究.| MgO | Mg(OH)2 | MgCO3 | |
| 消耗稀盐酸的体积/mL | 10.4 | 7.2 | 5.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 如图是甲、乙、丙三种固体物质的溶解度曲线,请回答:
如图是甲、乙、丙三种固体物质的溶解度曲线,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
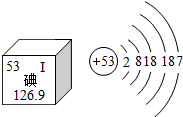
| A、碘的相对原子质量为126.9,原子核内质子数为53 |
| B、碘原子核外共有53个电子,最外层有7个电子 |
| C、碘原子在化学反应中容易得到电子 |
| D、碘盐中含有碘酸钾(KIO3),其中碘元素的化合价为-1价 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com