
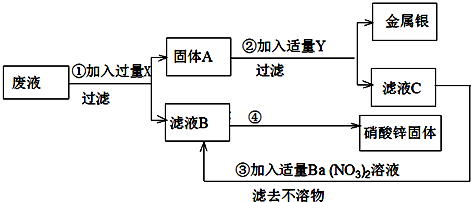
分析 根据废液主要含有Zn(NO3)2和AgNO3,为了从中回收金属银和硝酸锌,我们应该向其中加入过量的锌,这样既能回收银,又能保证滤液B中不含其它溶质,只有Zn(NO3)2.由于Zn是过量的,所以固体A中含有:Zn、Ag.为了把二者分开,我们可以加入过量的稀硫酸,让Zn与稀硫酸反应,然后过滤,从而回收银.滤液C中的硫酸锌我们可以向其中加入适量的硝酸钡溶液然后过滤得到液体B.为了得到Zn(NO3)2我们可以对其进行加热蒸发进行分析.
解答 解:(1)我们向废液中加入过量的锌,让锌与硝酸银反应Zn+2AgNO3═2Ag+Zn(NO3)2,然后过滤,得到固体A为(Zn、Ag)和液体B为 Zn(NO3)2溶液.为了把固体A中的银和锌分开,我们可以加入过量的Y即稀硫酸溶液,所以X是Zn,Y是H2SO4;
(2)固体A中加入过量Y即稀硫酸溶液后,其中锌与稀硫酸反应会生成硫酸锌,所以滤液C为硫酸锌溶液,所以固体A和滤液B、C中主要成分的化学式分别为:A:Ag和Zn;B:Zn(NO3)2;C:ZnSO4.;④中涉及的操作蒸发结晶;
(3)C是ZnSO4,硫酸锌与硝酸钡溶液反应生成硫酸钡沉淀和硝酸锌,③的化学方程式:ZnSO4+Ba(NO3)2=BaSO4↓+Zn(NO3)2
故答案为:
(1)Zn,H2SO4;
(2)Zn和Ag,Zn(NO3)2,ZnSO4.蒸发结晶;
(3)ZnSO4+Ba(NO3)2=BaSO4↓+Zn(NO3)2
点评 本题是一道推断题,要求学生能根据图表中的内容,恰当的选出所需要的物质,考查了学生的综合能力.是一道难度比较大的试题.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
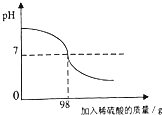 造纸厂生产会产生含氢氧化钠的废水,需经处理呈中性后排放.为测定此废水中氢氧化钠的质量分数,小华取80g废水样品加入到锥形瓶中,逐滴加入10%的稀硫酸,如图所示.
造纸厂生产会产生含氢氧化钠的废水,需经处理呈中性后排放.为测定此废水中氢氧化钠的质量分数,小华取80g废水样品加入到锥形瓶中,逐滴加入10%的稀硫酸,如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com