
金属和金属材料在生活、生产中应用广泛。
(1)铁在潮湿的空气中容易生锈,实际上是与空气中的_____________等发生了化学反应;
(2)用Fe、Ag和________溶液(填序号),可以一次性验证Fe、Cu、Ag三种金属的活动性顺序。写出有关反应的化学方程式___________________________。
①AgNO3溶液 ②CuSO4溶液; ③Al2(SO4)3溶液
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源:2017届广东省汕头市龙湖区九年级5月模拟考试化学试卷(解析版) 题型:探究题
如图1所示是实验室制取气体的装置,请回答:
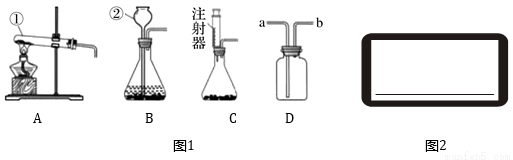
(1)写出有标号仪器的名称:①_________;②_________;
(2)实验室用氯酸钾和二氧化锰制取氧气,反应的化学方程式为________________。若用D装置来收集氧气,气体应从_______(填“a”或“b”)端进入;
(3)在实验室里,二氧化碳常用石灰石与稀盐酸反应来制取.若要控制反应速率和节约药品,应选用的发生装置为_______(填序号);
(4)①用质量分数为37%的浓盐酸配制100g 10%的盐酸,除了用到胶头滴管、玻璃棒和和量筒外,还需补充的一种仪器是___________;
②将上述配制好的溶液装入试剂瓶中,盖好瓶塞并贴上标签。请在如图2所示的标签内填入相应的内容。_________
查看答案和解析>>
科目:初中化学 来源:2017届广东省汕头市龙湖区九年级5月模拟考试化学试卷(解析版) 题型:选择题
水是生命之源,下列有关水的说法不正确的是( )
A.水的电解实验说明水是由氢气和氧气组成的
B.生活中通过煮沸的方法可以降低水的硬度
C.用蒸馏的方法可以将海水淡化
D.爱护水资源主要从节约用水和防治水体污染两方面采取相应措施
查看答案和解析>>
科目:初中化学 来源:2017届山东省日照市莒县九年级下学期第二次学业水平模拟测试化学试卷(解析版) 题型:信息分析题
在一次用餐中,同学们对“固体酒精”产生了好奇,于是对其成分进行研究。
【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成。(2)氯化钙、氯化钡溶液均呈中性。
【提出问题】(1)酒精中是否含有碳元素?
(2)固体酒精中的氢氧化钠是否变质?
【实验探究】(1)按如图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论,此结论_____(选填“合理”或“不合理”)。
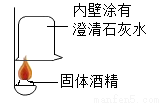
(2)为确定氢氧化钠的变质程度,分组探究。取少量固体酒精于烧杯中,加足量的水充分溶解后静置。
①甲组按下表探究:
实验步骤 | 实验现象 | 结论 |
取上层清液于试管中,滴加酚酞溶液 | 溶液变红 | 清液中有氢氧化钠 |
取上层清液于另一试管中,加入适量氯化钡溶液 | _____ | 清液中有碳酸钠 |
②乙组认为甲组实验不能证明清夜中一定有氢氧化钠,理由是______________。他们另取烧杯中上层清夜,加足量氯化钡溶液,充分反应后滴加酚酞溶液,酚酞溶液变红。
【实验结论】经讨论一致认为固体酒精中的氢氧化钠部分变质。
【拓展应用】要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的___(填序号)
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液
查看答案和解析>>
科目:初中化学 来源:2017届山东省日照市莒县九年级下学期第二次学业水平模拟测试化学试卷(解析版) 题型:选择填充题
物质的宏观性质与微观组成(或结构)相互联系是化学特有的思维方式, 下列对物质性质的微观解释不正确的是( )
A. 降温能使水结冰,是因为在较低的温度下水分子静止不动
B. 水和过氧化氢化学性质不同,是因为分子的构成不同
C. 稀有气体的化学性质比较稳定,是因为它们的原子结构都相对稳定
D. 氢氧化钾溶液、石灰水都能使石蕊试液变蓝,是因为它们都含有OH-
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 ”为铜片).
”为铜片).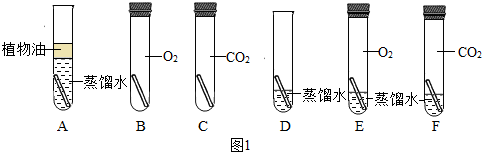
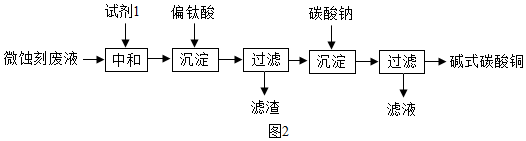
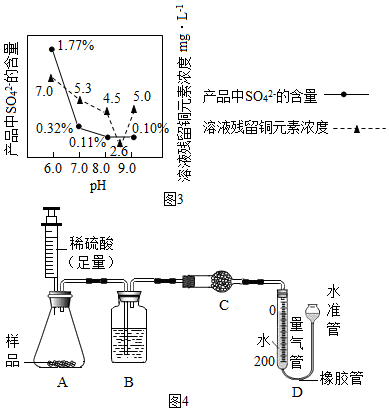
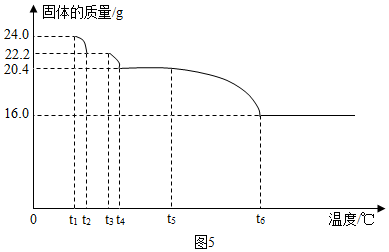
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
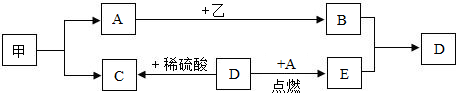
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com