
(5分)某学习小组用右图装置测定铜锌合金中锌、铜的质量分数。
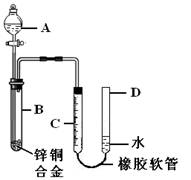
(1)B中发生的化学反应方程式为 ;
(2)主要实验操作步骤有:检查气密性,将药品和水装入各仪器中,连接好装置后,再进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥,称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B滴加足量试剂。上述操作的顺序是 (填序号);
(3)若实验用铜锌合金的质量为ag,与酸充分反应后,测得氢气体积为VL,为求出合金中锌、铜的质量分数,还缺少的一个数据是 (填字母);
A. 反应前加入稀酸的体积 B. 反应前加入稀酸的质量分数
C. 实验前反应装置中空气的体积 D. 实验条件下氢气的密度
(4)若实验用铜锌合金的质量为ag,与酸充分反应后,B中剩余固体的质量为bg,则锌的质量分数为 ;
(5)实验过程中,若未洗涤过滤所得的不溶物,则得到锌的质量分数将 (填“偏大”、“偏小”或“不受影响”)。
32. (5分,每空l分。)
(1)Zn+2HCl ZnCl2+H2↑(或Zn+H2SO4 ZnSO4+H2↑)
(2)①④③②
(3)D
(4)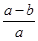 ×100%
×100%
(5)偏小
【解析】
试题分析:(1)B中发生的化学反应方程式为Zn+2HCl ZnCl2+H2↑(或Zn+H2SO4 ZnSO4+H2↑);
(2)主要实验操作步骤有:检查气密性,将药品和水装入各仪器中,连接好装置后,再①记录C的液面位置;④由A向B滴加足量试剂;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥,称重;
(3)根据化学方程式可以计算Zn的质量,从而计算出Zn的质量分数,但带入化学方程式计算的应该是物质的质量,题中只有氢气的体积,故还缺少氢气的密度;
(4)(4)若实验用铜锌合金的质量为ag,与酸充分反应后,B中剩余固体的质量为bg,则锌的质量分数为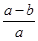 ×100%
×100%
(5)实验过程中,若未洗涤过滤所得的不溶物,则所得不溶物上沾有水,其质量偏大,故得到锌的质量分数将偏小。
考点:化学方程式;实验探究;根据化学方程式计算;质量分数的计算。
点评:本题由给定装置图来探究金属质量分数,首先要读懂图的含义,难度较大。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
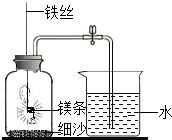 某校研究性学习小组用右图装置进行镁条在空气中燃烧的实验.先将镁条燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
某校研究性学习小组用右图装置进行镁条在空气中燃烧的实验.先将镁条燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.查看答案和解析>>
科目:初中化学 来源: 题型:
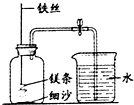 某校研究性学习小组用右图装置(气密性良好)进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.
某校研究性学习小组用右图装置(气密性良好)进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.查看答案和解析>>
科目:初中化学 来源:2011届北京市昌平区中考二模化学试卷 题型:探究题
(5分)某学习小组用右图装置测定铜锌合金中锌、铜的质量分数。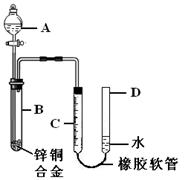
(1)B中发生的化学反应方程式为 ;
(2)主要实验操作步骤有:检查气密性,将药品和水装入各仪器中,连接好装置后,再进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥,称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B滴加足量试剂。上述操作的顺序是 (填序号);
(3)若实验用铜锌合金的质量为ag,与酸充分反应后,测得氢气体积为VL,为求出合金中锌、铜的质量分数,还缺少的一个数据是 (填字母);
| A.反应前加入稀酸的体积 | B.反应前加入稀酸的质量分数 |
| C.实验前反应装置中空气的体积 | D.实验条件下氢气的密度 |
查看答案和解析>>
科目:初中化学 来源:2008-2009学年广东省佛山市高明区九年级(上)期末化学试卷(解析版) 题型:解答题
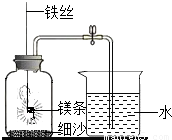
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com