
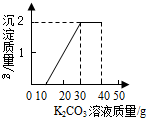
 某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40mL该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如图所示.求:
某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40mL该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如图所示.求: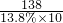 =
=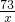 =
=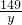
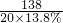 =
=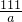 =
=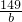 =
=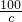


科目:初中化学 来源: 题型:
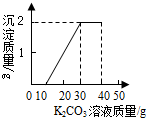 某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40mL该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如图所示.求:
某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40mL该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如图所示.求:查看答案和解析>>
科目:初中化学 来源: 题型:
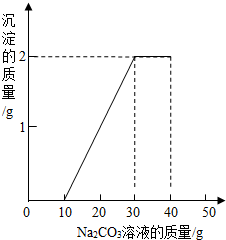 某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合液(不考虑其他杂质)进行如下实验:取一定量该混合液于烧杯中,滴加40g溶质质量分数为10.6%的碳酸钠溶液后,称得烧杯内溶液总质量为68.5g.滴入碳酸钠溶液的质量与生成沉淀质量关系如图所示.
某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合液(不考虑其他杂质)进行如下实验:取一定量该混合液于烧杯中,滴加40g溶质质量分数为10.6%的碳酸钠溶液后,称得烧杯内溶液总质量为68.5g.滴入碳酸钠溶液的质量与生成沉淀质量关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:
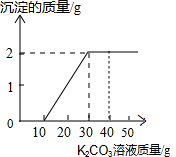 某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40g该溶液于烧杯中,滴入40g溶质质量分数为 13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如如图所示.回答下列问题:(最后结果保留1位小数)
某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40g该溶液于烧杯中,滴入40g溶质质量分数为 13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如如图所示.回答下列问题:(最后结果保留1位小数)查看答案和解析>>
科目:初中化学 来源: 题型:
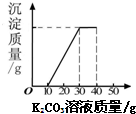 某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40mL该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如右图所示.求:
某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40mL该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如右图所示.求:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com