
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:(1)根据由非金属元素组成的气态非金属单质一般是由分子构成的;氧气由双原子分子构成,表示为:O2;
(2)氩是稀有气体元素,由稀有气体元素组成的单质是单原子分子,所以氩气的化学式就是表示氩元素的元素符号,因此表示为:Ar;
(3)红磷的化学式为:P;
(4)镁条的化学式为:Mg;
(5)氧化铁是由显+3价的铁元素和显-2价的氧元素组成,根据化合价原则,其化学式为:Fe2O3;
(6)根据化合物的读法,Na2SO4读作硫酸钠;
(7)根据化合物的读法,N2O5读作五氧化二氮;
故答案为:(1)O2(2)Ar(3)P (4)Mg (5)Fe2O3(6)硫酸钠 (7)五氧化二氮
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
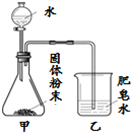 “食品蒸汽加热器”常用于野外加热食物.加热袋中的固体粉末含镁粉、铁粉和氯化钠,使用时向其中加入水袋中的水,即可产生大量热.实验小组针对放热过程中的反应原理展开探究.
“食品蒸汽加热器”常用于野外加热食物.加热袋中的固体粉末含镁粉、铁粉和氯化钠,使用时向其中加入水袋中的水,即可产生大量热.实验小组针对放热过程中的反应原理展开探究.| 实验序号 | A | B | C | D | E | F |
| 固体成分 | Mg | Fe | Mg+Fe | Mg+NaCl | Fe+NaCl | Mg+Fe+NaCl |
| 乙中现象 | 少量肥皂泡,难以点燃 | ① | 少量肥皂泡,难以点燃 | 较多肥皂泡,点燃有爆鸣声 | 无肥皂泡 | 大量肥皂泡, 点燃有爆鸣声 |
| 混合物温度 | 23.1℃ | 22.8℃ | 23.1℃ | 24.2℃ | 22.8℃ | 27.2℃ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铜是人类最早利用的金属材料 | |
| B. | 铁是目前世界年产量最高的金属 | |
| C. | 大多数金属元素在自然界中以单质形式存在 | |
| D. | 日常使用的金属材料大多数是合金 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用10mL的量筒量取9.0mL水 | |
| B. | 用100mL的量筒量取2.0mL水 | |
| C. | 用托盘天平称取10.58g碳酸钠粉末 | |
| D. | 用150mL酒精和50mL水精确配制200mL医用消毒酒精 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
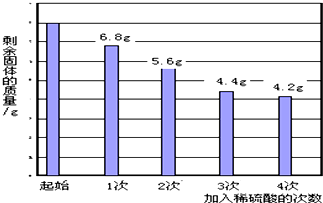 现有铜与金属镁、铁、锌中的一种组成的混合物,兴趣小组的同学欲测定其组成.进行以下实验,取该混合物粉末8.0g放入烧杯中,将140.0g 溶质的质量分数为14.0%的稀硫酸平均分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如图.请你通过计算回答:
现有铜与金属镁、铁、锌中的一种组成的混合物,兴趣小组的同学欲测定其组成.进行以下实验,取该混合物粉末8.0g放入烧杯中,将140.0g 溶质的质量分数为14.0%的稀硫酸平均分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如图.请你通过计算回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com