


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
| A、3:7 | B、7:3 |
| C、77:81 | D、81:77 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、正盐可能含氢元素 |
| B、酸和碱的组成中一定含氢元素和氧元素 |
| C、酸、正盐、酸式盐一定含氢元素 |
| D、酸、碱、盐都可能不含金属元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、原子是化学变化中最小的粒子 |
| B、原子都是由质子、中子、电子构成 |
| C、原子核带正电荷,但原子不显电性 |
| D、在原子中,核电荷数=质子数=电子数 |
查看答案和解析>>
科目:初中化学 来源: 题型:
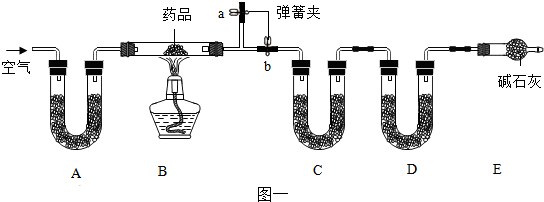
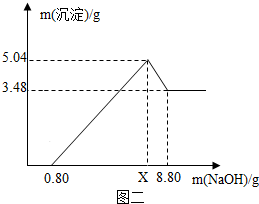
查看答案和解析>>
科目:初中化学 来源: 题型:
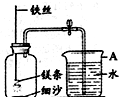 某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.查看答案和解析>>
科目:初中化学 来源: 题型:
 A、B、C三种固体物质的溶解度如右图所示,根据图答题:
A、B、C三种固体物质的溶解度如右图所示,根据图答题:查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验序号 | 过氧化氢溶液 | 催化剂 | 温度 | 氧气体积 | 待测数据 |
| Ⅰ | 50mL l0% | 8g MnO2 | 常温 | 100mL | |
| Ⅱ | 50mL l0% | 8g A | 常温 | 100mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com