(2012?北京)同学们发现NaOH溶液与NaHCO
3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO
3溶液与NaOH溶液发生了反应.
(1)实验装备
①查阅资料:NaHCO
3+NaOH═Na
2CO
3+H
2O
②用一定溶质的质量分数的NaHCO
3、NaOH和Na
2CO
3三种溶液进行如下实验,为设计实验方案提供参考.
|
NaHCO3溶液 |
NaOH溶液 |
Na2CO3溶液 |
| 加入稀盐酸 |
现象Ⅰ |
无明显变化 |
产生气泡 |
| 加入澄清石灰水 |
溶液变浑浊 |
无明显变化 |
现象Ⅱ |
| 加入CaCl2溶液 |
无明显变化 |
溶液变浑浊 |
溶液变浑浊 |
加热溶液至沸腾,将
气体通入澄清石灰水 |
澄清石灰水
变浑浊 |
澄清石灰水
无明显变化 |
澄清石灰水
无明显变化 |
表中的现象Ⅰ为
有气泡产生
有气泡产生
,现象Ⅱ对应反应的化学方程式为
Ca(OH)2+Na2CO3=2NaOH+CaCO3↓
Ca(OH)2+Na2CO3=2NaOH+CaCO3↓
.
(2)实验过程
【实验1】证明反应生成了Na
2CO
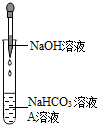
3同学们选用上表实验中的药品,设计了如右图所示实验,先在NaHCO
3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是
CaCl2
CaCl2
.
有同学提出这个实验不足以证明有Na
2CO
3生成,其理由是
CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀
CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀
.为了证明有Na
2CO
3生成,需要继续进行的操作是
取少量反应后滤渣加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有
取少量反应后滤渣加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有
.
【实验2】证明反应后NaHCO
3不存在
同学们参考上表中的实验,又设计了一个实验,虽然没有观察到明显的实验现象,但可以证明反应发生了,该实验方案是
取少量反应后的溶液加热至沸腾,将气体通入澄清石灰水,若澄清石灰水变浑浊,证明有:NaHCO3存在,反之则没有.
取少量反应后的溶液加热至沸腾,将气体通入澄清石灰水,若澄清石灰水变浑浊,证明有:NaHCO3存在,反之则没有.
.
(3)实验反思
通过实验1和实验2说明,对于没有明显现象的化学反应,可以从两个不同的角度证明反应的发生,这两个角度是
一是可以通过检验反应物证明反应发生,二是可以通过检验产物证明反应发生
一是可以通过检验反应物证明反应发生,二是可以通过检验产物证明反应发生
.



 (2012?北京)同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
(2012?北京)同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.