(2006?泰安)小明在“探究盐酸和氢氧化钙能否发生化学反应”时,设计了如图所示的对照实验:
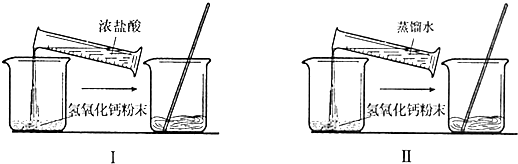
他设想在室温下,先取少量氢氧化钙粉末分别放入两只烧杯中,在Ⅱ烧杯中加入一定量的蒸馏水,在I烧杯中加入含等量蒸馏水的浓盐酸,充分搅拌,一段时间后,观察现象.
根据上述情况,请回答以下问题:
(1)你认为要得到可靠的实验结论,需要保证实验I、Ⅱ中
氢氧化钙粉末的质量
氢氧化钙粉末的质量
完全相同.预测通过观察
实验I中白色粉末消失成为无色溶液或(实验I中的浑浊程度比实验Ⅱ中小)
实验I中白色粉末消失成为无色溶液或(实验I中的浑浊程度比实验Ⅱ中小)
的现象,说明盐酸和氢氧化钙发生了化学反应;
(2)设计对照实验Ⅱ的目的是
排除氢氧化钙粉末溶于水的因素,以证实氢氧化钙粉末与盐酸发生化学反应
排除氢氧化钙粉末溶于水的因素,以证实氢氧化钙粉末与盐酸发生化学反应
;
(3)如果不采用对照实验,请你设计一个简单实验证明盐酸和氢氧化钙能够发生化学反应:
在一定量的氢氧化钙粉末中加入适量的水,再滴加2--3滴酚酞试液,浑浊液变红,然后加入适量盐酸至红色消失,变为无色液体,说明盐酸与氢氧化钙能够发生化学反应
在一定量的氢氧化钙粉末中加入适量的水,再滴加2--3滴酚酞试液,浑浊液变红,然后加入适量盐酸至红色消失,变为无色液体,说明盐酸与氢氧化钙能够发生化学反应
;
(4)写出该反应的化学方程式
Ca(OH)2+2HCl=CaCl2+2H20
Ca(OH)2+2HCl=CaCl2+2H20
.



