3.烧碱的用途很广,工业上制得的烧碱中常含有杂质碳酸钠,某化学兴趣小组同学对购买的烧碱成分和纯度测定展开了讨论与探究.
(1)为检验烧碱中是否含有碳酸钠,同学们提出不同方案.
方案一:配成溶液,向其中滴加酚酞试液.同学们认为该方法无法检验,原因是两种溶液都呈碱性.
方案二,配成溶液,向其中慢慢滴加稀盐酸,大家发现,刚开始滴加时无气泡产生,原因是NaOH+HCl=NaCl+H
2O (用化学方程式表示).
方案三:配成溶液,向其中滴加一种盐的溶液,可以证明含有碳酸钠,该溶液是BaCl
2、(或CaCl
2、Ca(NO
3)
2等).
(2)测定烧碱的纯度
实验原理:利用Na
2CO
3与稀H
2SO
4反应产生CO
2,通过测定CO
2的质量,确定样品中碳酸钠的质量,从而计算样品的纯度.
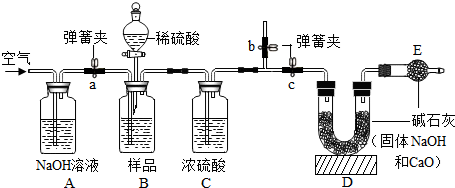
①学们根据实验原理,设计了如图的实验(固定装置省略),装置A的作用是除去空气中的CO
2.
②B装置中样品在与稀硫酸反应前和停止反应后,都要通入过量的空气.反应前通空气的目的是排出装置中的CO
2.停止反应后,若不再通入空气,则测得工业烧碱的纯度将偏高(填“偏高”“偏低”或“无影响”).
③若撤去C装置,则测得工业烧碱的纯度将偏低(填“偏高”“偏低”或“无影响”).
④D、E中都放入碱石灰,其中,E中碱石灰的作用是防止空气中的水和二氧化碳进入D装置.
⑤现取50克样品,按照图中正确的实验方法测定,待无气泡产生时,称得C装置增重0.6克,D装置增重2.2克,试通过计算,推测样品中烧碱的纯度?(有计算过程,精确到0.1%)
⑥反思:若用上面的烧碱配制氢氧化钠溶液,需除去其中的碳酸钠,除去的方法很多,比如,向该样品配制的溶液中加入适量Ca(OH)
2 溶液,过滤,即得到氢氧化钠溶液.


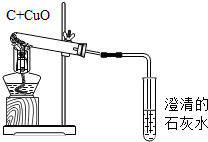 根据如图回答下列问题;
根据如图回答下列问题;