
【题目】某化学学习小组利用下图设计方案来探究可燃物燃烧的条件。

(1)此实验主要利用了铜的什么物理性质?______________
(2)按上图进行实验,可得出的实验结论是什么?______________
(3)实验后小亮发现铜片变黑了,质量也变大了。请解释原因。______________
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:初中化学 来源: 题型:
【题目】苹果中富含苹果酸,具有增强消化,降低有害胆固醇等作用,苹果酸的分子式 为 C4H6O5 请计算:
(1)苹果酸的相对分子质量是_____
(2)苹果酸中碳、氢、氧三种元索的质量比是____(最简整数比)
(3)13.4g 苹果酸中含 C 元素质量_________克?(写出计算过程,答案精确到 0.1)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小王在市场看到,鱼老板将一勺白色粉末加入水中,水中奄奄一息的鱼很快张开嘴,活蹦乱跳起来,小王对这种“白色粉末”很感兴趣,就进行了相关探究。
(查阅资料)这种“白色粉末”的成分是过氧化钙(化学式为CaO2),常温下,CaO2能与水慢慢反应生成氧气。
⑴小王选用如下图所示装置中的_____选填序号)进行过氧化钙与水的反应并收集产生的气体,经检验该气体是氧气,验满的方法是_______________________________________ 。
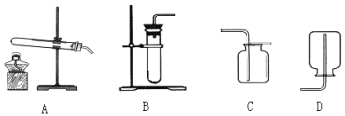
(提出问题)过氧化钙与水反应得到溶液M中溶质的成分是什么?小王进行以下实验探究:
⑵(猜想假设)根据过氧化钙与水的组成作出了猜想溶质的成分是_________(化学式)。
⑶(实验验证)小王取溶液M适量置于试管中,向溶液M中滴入_______,溶液变红色。再另取溶液M,向其中通入____气体观察到有白色沉淀生成,则小王的猜想正确。
⑷过氧化钙与水反应的方程式为:___________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】按要求写出化学用语或化学用语所表示的意义。
(1)氯酸钾____________________ (3)标出氧化铝中铝元素的化合价_______________(3)2H______________________ (4)3N2__________________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸钠在生活和生产中都有广泛的用途。为探究碳酸钠的化学性质,同学们做了如下实验。
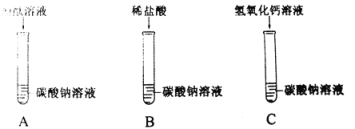
请根据实验回答问题。
(1)A试管中溶液变成红色,说明碳酸钠溶液显______________性。
(2)B试管中观察到的实验现象为_____________________,说明碳酸钠能与盐酸反应。
(3)C试管中有白色沉淀产生,写出该反应的化学方程式__________________________。实验结束后,同学们将三支试管中的物质倒入同一个洁净的烧杯中,静置段时间后,观察到烧杯底部有白色沉淀,上层溶液为无色。
(提出问题)无色溶液中除酚酞外还有哪些溶质?
(分析讨论)无色溶液中一定含有的溶质是______________(填化学式,下同);可能含有的溶质是______________。
(实验验证)为检验无色溶液中可能含有的溶质是否存在,请你帮助他们设计实验方案___________(写出实验操作、现象及结论)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】元素化学性质与最外层电子数有密切关系。钾原子的结构示意图为![]() ,下图表示的微粒中共有_________种元素,其中与钾原子具有相似化学性质的是_______,B与C形成化合物的化学式为__________。
,下图表示的微粒中共有_________种元素,其中与钾原子具有相似化学性质的是_______,B与C形成化合物的化学式为__________。
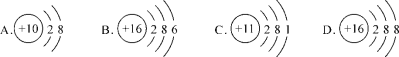
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像正确的是
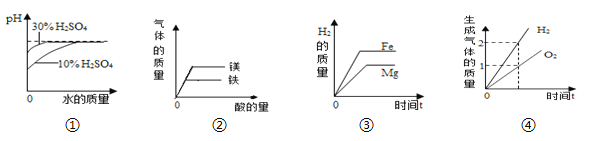
A. 图①:稀释等质量的30%H2SO4和10%H2SO4溶液
B. 图②:分别往等质量的Mg和Fe中滴加足量稀H2SO4
C. 图③:将等质量的Mg和Fe投入到足量稀H2SO4中
D. 图④:电解水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国劳动人民早在五千年前就会使用木炭炼铜.在化学实验室里模拟炼铜,既可用传统的实验装置(见图甲),又能用改进的微型实验装置(见图乙).化学兴趣小组采用图乙装置,开展以下探究活动
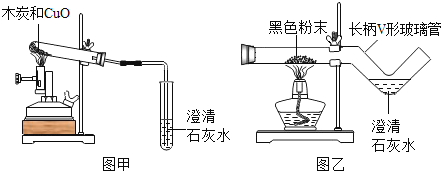
(提出问题)木炭与CuO反应所得红色固体中含有什么物质?
(查阅资料)(1)木炭与CuO的反应是:C+2CuO![]() 2Cu+CO2↑,若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O).
2Cu+CO2↑,若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O).
(2)Cu2O是红色固体,能与稀硫酸反应:Cu2O+H2SO4====Cu+CuSO4+H2O
(作出猜想)红色固体的成分:①全部是Cu;②全部是Cu2O;③_______________.
(实验探究)
(1)取木炭、CuO两种黑色粉末适量,再加少许CaC12(能降低反应温度,加快反应速率)均匀混合,然后将黑色粉末装入长柄V形玻璃管的直管内.
(2)按图乙连好实验装置,____________,然后加热反应物;2分钟后,黑色粉末出现红热现象,同时澄清的石灰水_______________,此时停止加热。
(3)待玻璃管冷却后,提取里面的红色固体,进行如下的验证:
步骤 | 现象 | 结论 |
①取2.88g红色固体装入试管,滴入足量 的_______________,充分反应 | 红色固体部分减少,溶液变 为_______________色 | 猜想____错误 |
②滤了试管中残留的红色固体,洗涤干燥 称其质量为2.08g | 猜想____正确 |
(评价反思)
(1)使用图乙装置与使用图甲装置相比,其优点是_______________(写出1条即可);
(2)要证明氯化钙CaCl2是催化剂还需要验证CaCl2反应前后__________________不变.
(拓展提高)
我们生活中的铜有一部分是由辉铜矿(主要成分为硫化亚铜(Cu2S))的矿石冶炼而成,经测定该矿石由硫化亚铜(Cu2S)和其他不含铜元素的物质组成.现用100g该矿石制得2.16g纯氧化亚铜(Cu2O),该纯氧化亚铜(Cu2O)中铜元素的质量是__________g.若制得氧化亚铜(Cu2O)的过程中,铜元素的总损耗为20%,通过计算确定该矿石中硫化亚铜(Cu2S)的质量分数_________?(请写出计算过程).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】南海是我国五大海区中最大的海区,自然海区总面积约为350万平方公里,海洋资源丰富,开发前景十分远大。
(1)海洋中有大量的鱼、虾,食用海鱼、海虾可为人体提供的营养素主要是____。(填序号)
A. 糖类 B.蛋白质 C. 维生素 D.油脂
(2)海水中蕴藏着丰富的食盐资源,目前从海水中提取食盐的方法主要为_________
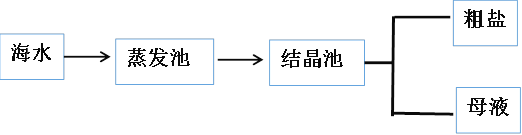
上述过程得到的粗盐属于 ___________(填“纯净物”或“混合物”)。
(3)从海水中可以提取金属镁,金属镁广泛应用于火箭、导弹和飞机制造业。目前世界上60%的镁是从海水(主要含NaCl和MgC2等)中提取的,主要步骤如下:
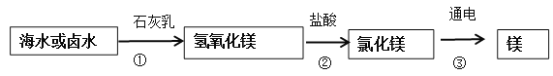
海水中本身就含有氯化镁,则①②两步的作用是 ______________。
(4)海底不仅蕴藏着大量的煤、石油、天然气等常规化石燃料,人们还在海底发现了一种新型矿产资源——“可燃冰”。下列有关“可燃冰”的说法正确的是_________ 。
A.是可再生能源
B.燃烧产物只有水,无污染
C.蕴藏量大,热值大,燃烧后几乎不产生任何残渣和废气,被誉为“未来能源”
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com