
重铬酸钾(K2Cr2O7Mr=294,铬元素为+6价,Mr表示相对分子质量)是一种重要的化工原料,在皮革工业、有机反应中都有广泛应用.但+6价格有很强的毒性易污染环境,使用后,须用绿矾,(FeSO4?7H2O,Mr=278)将其变成毒性+3价格才能做后续处理.反应原理是:6FeSO4?7H2O+K2Cr2O7+7H2SO4═3Fe2(SO4)3+Cr2(SO4)3+K2SO4+49H2O现有1.0吨重铬酸钾需要处理,计算需绿矾多少吨?(写出计算过程,结果精确到小数点后1位)
科目:初中化学 来源: 题型:单选题
现有100g过氧化氢溶液,测得其中含氢元素的质量分数为8%,加入8gCuSO4作催化剂
制取氧气,充分反应后所得溶液(无晶体析出)中溶质的质量分数为
| A.7.4% | B.10% | C.8% | D.11.1% |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
早在西汉时期,我国就用铁与硫酸铜溶液反应制取铜,称为“湿法炼铜”。
(1)请写出“湿法炼铜”的化学方程式 。
(2)若用该方法制得铜32 g,反应的铁的质量为 g,若同时消耗了500 g硫酸铜溶液,则该硫酸铜溶液中硫酸铜的质量分数为 %。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(5分)现有20 g含Fe2O3为80%的赤铁矿石,加入到150 g稀盐酸中,恰好完全反应(铁矿石中的杂质都不溶于水,且不与稀盐酸反应)。(计算结果保留一位小数)
求:(1)赤铁矿石中Fe2O3的质量为 g, Fe2O3中铁元素的质量为 g;
(2)稀盐酸中溶质的质量分数;
(3)恰好完全反应后所得溶液中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(6分) 有资料表明,氧化铜代替二氧化锰加入氯酸钾中也能很快产生氧气.先将2.4g氧化铜与wg氯酸钾的混合物充分加热,使其不再产生气体后,残余固体经冷却、称量,质量为wg.然后将固体溶于21.3g水中,充分搅拌,过滤,得到滤液和黑色的滤渣.滤渣又经洗涤、烘干、称量,质量为2.4g。(注:不考虑每步实验过程中物质的损失;计算结果保留1位小数)
(1)该反应中氧化铜起 作用。
(2)求生成的O2质量;
(3)求所得的滤液溶质的质量分数.
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
100克某浓度的硫酸恰好与13克的锌完全起反应,请计算:
(1)生成氢气的质量(结果精确到0.1g).
(2)将(1)的结果标在图中;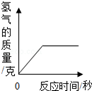
(3)反应后所得溶液中溶质的质量分数(写出计算过程,结果精确到0.1%).
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(10分)金属过氧化物等可作宇宙飞船或潜水艇中的氧气再生剂,如:过氧化钠(Na2O2)在常温下能与人呼出的二氧化碳反应生成氧气,化学方程式为:2Na2O2+2CO2===2Na2CO3+O2↑。为了验证该反应中氧气的产生,某兴趣小组的同学设计了如图所示的实验。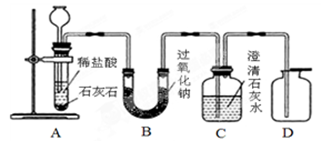
(1)A装置中所发生反应的化学方程式为 ;实验室确定气体发生装置时应考虑的因素是 ;检查A装置的气密性的方法是:将A装置中导气管上的胶皮管用弹簧夹夹住,往长颈漏斗中注入水至液面高出漏斗颈的下端管口,若能观察到 现象,即可证明装置不漏气。
(2)表明二氧化碳没有被过氧化钠完全吸收的现象是 。
(3)用带火星的木条放在集气瓶口检验氧气是否收集满,这是利用了氧气性质中的 ;
(4)如果用脱脂棉包裹一定量的Na2O2固体,然后向其中通入CO2,脱脂棉很快就燃烧此现象说明该反应为 反应(填“吸热”或“放热”);
(5)常温下水也能与Na2O2反应生成氧气和氢氧化钠,该反应的化学方程式为2Na2O2+2H2O===4NaOH+O2↑,若要检验干燥的二氧化碳能否与过氧化钠反应生成氧气,对以上实验装置的改进为
(6)实验室中的过氧化钠如果保存不当,容易与空气中的CO2和水蒸汽发生反应变质。今称取10g过氧化钠样品(杂质不参加反应)放人烧杯中,向其中加入10g水,二者完全反应后。称量烧杯中剩余物质的总质量为18.4g(不包括烧杯的质量,且气体的溶解忽略不计)。试计算过氧化钠样品中杂质的质量分数(要写出计算过程)。(3分)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(3分)为测定NaCl和Na2SO4固体混合物中NaCl的质量分数,化学小组同学进行如下实验活动: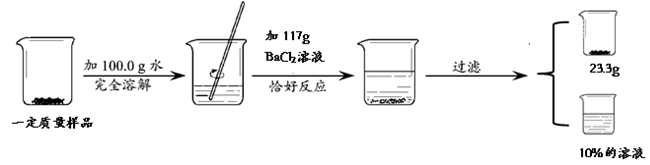
由此测得原固体混合物中NaCl的质量分数是多少?(已知:Na2SO4 + BaCl2 ===BaSO4↓ + 2NaCl)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(7分) 工业上常用稀盐酸处理铁制品表面的铁锈,据此请回答下列问题:
(1)除去铁锈的过程中还可以看到的一项实验现象是______________________________;
(2)如果稀盐酸用量太多就会看到有气泡产生,用化学方程式说明原因:
____________________________________________;
(3)工业上用了30千克溶质质量分数为7.3%的稀盐酸,与某铁制品表面的铁锈恰好完全反应,求反应后溶液的质量。(计算结果精确到小数点后一位)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com