
| 实验 操作 | 实验现象 | 结论 |
| ①用少量粉末装入试管,加少量蒸馏水溶解,向溶液中滴加足量的盐酸,并不断震荡 | 现象A | 猜 想2不成立 |
| ②取步骤①中少量的液体于试管中然后,操作Ⅱ | 有白色沉淀 | 猜想1不成立 |
| 实验 操作 | 实验现象 | 结论 |
| ①用少量粉末装入试管,加少量蒸馏水溶解,向溶液中滴加足量的盐酸,并不断震荡 | 现象A | 猜 想2不成立 |
| ②取步骤①中少量的液体于试管中然后,操作Ⅱ | 有白色沉淀 | 猜想1不成立 |


科目:初中化学 来源: 题型:
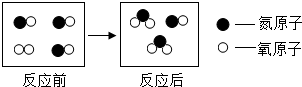
 和
和 生成的质量比为
生成的质量比为查看答案和解析>>
科目:初中化学 来源: 题型:
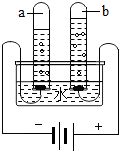 有关电解水实验的叙述,(如图所示)错误的是( )
有关电解水实验的叙述,(如图所示)错误的是( )| A、在水中加入少量的稀硫酸是为了增强水的导电性 |
| B、与电源正极相连的玻璃管内得到的气体能在空气中燃烧 |
| C、该实验证明水是由氢元素和氧元素组成 |
| D、试管a与试管b中产生的气体体积比约为2:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、家用电器着火,用水扑灭 |
| B、木材着火,立即用水扑灭 |
| C、浓硫酸沾到皮肤上,用氢氧化钠溶液冲洗 |
| D、一氧化碳泄漏,立即放一盆水吸收 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 奇思妙想化学兴趣小组的同学们在探究物质燃烧的条件时,用一个集气瓶罩住燃着的小蜡烛,小蜡烛一会儿就熄灭了.它为什么会熄灭呢?每个人都提出了不同的猜想.
奇思妙想化学兴趣小组的同学们在探究物质燃烧的条件时,用一个集气瓶罩住燃着的小蜡烛,小蜡烛一会儿就熄灭了.它为什么会熄灭呢?每个人都提出了不同的猜想.| 实验步骤 | 实验现象 | 实验分析 | 实验结论 |
| (1)取一小块白磷(着火点为40°C),放在一铝箔制的小盒中,然后放入装有生石灰的集气瓶内.点燃蜡烛,塞紧胶塞,观察现象. | 燃烧的蜡烛一会儿就熄灭了. | 白磷燃烧需满足的条件: ①温度达到着火点; ② | 小龙的猜想是正确的. |
| (2)待冷却后,打开分液漏斗活塞,向集气瓶中注入少量水,立即关闭活塞,观察现象. | 铝盒中的白磷燃烧, 放出热量的同时产 生了 |
查看答案和解析>>
科目:初中化学 来源: 题型:
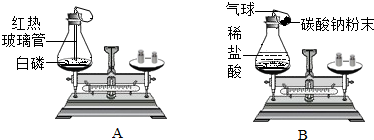
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、H2SO4+CuO═CuSO4+H2O |
| B、H2SO4+Cu(OH)2═CuSO4+2H2O |
| C、CaCO3+2HCl═CaCl2+H2O+CO2↑ |
| D、Ca(OH)2+CO2═CaCO3↓+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:
 溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据如图的溶解度曲线填空.
溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据如图的溶解度曲线填空.查看答案和解析>>
科目:初中化学 来源: 题型:
| A、MgCl2溶液 |
| B、H2SO4溶液 |
| C、CuCl2溶液 |
| D、酚酞试液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com