
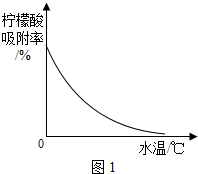
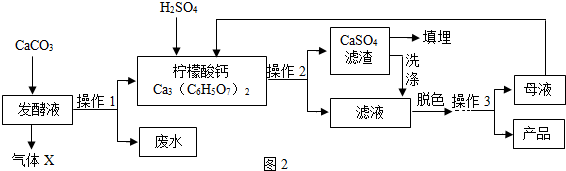
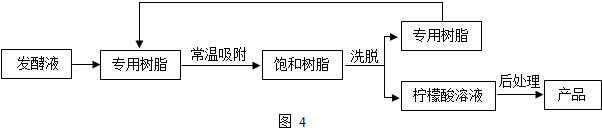
 柠檬酸(C6H8O7)是一种工业原料,广泛应用于食品、医药等行业,如图2、4是两种不同方法制备一水柠檬酸晶体C6H8O7?H2O)的工艺流程图,回答相关问题:
柠檬酸(C6H8O7)是一种工业原料,广泛应用于食品、医药等行业,如图2、4是两种不同方法制备一水柠檬酸晶体C6H8O7?H2O)的工艺流程图,回答相关问题:| 温度/℃ | 0 | 10 | 20 | 30 | 40 | … |
| 溶解度/g | 96 | 118 | 146 | 183 | 216 | … |


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
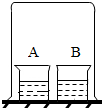 某兴趣小组以下实验探究分子的运动.请回答实验中的有关问题:如图所示,A中盛有浓盐酸,B中盛有滴加酚酞的氢氧化钠溶液,放置一段时间,观察到烧杯B中的现象是
某兴趣小组以下实验探究分子的运动.请回答实验中的有关问题:如图所示,A中盛有浓盐酸,B中盛有滴加酚酞的氢氧化钠溶液,放置一段时间,观察到烧杯B中的现象是查看答案和解析>>
科目:初中化学 来源: 题型:
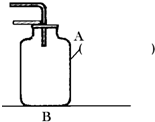 实验室用稀盐酸和大理石制取二氧化碳气体:
实验室用稀盐酸和大理石制取二氧化碳气体:查看答案和解析>>
科目:初中化学 来源: 题型:
| 饮酒驾车 | 20毫克/100毫升≤血液中的酒精含量<80毫克/100毫升 |
| 醉酒驾车 | 血液中的酒精含量≥80毫克/100毫升 |
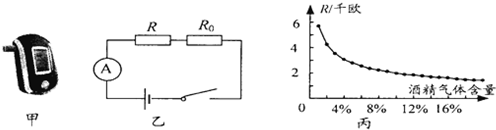
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
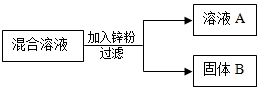 某化学小组用一定量AgNO3和Cu(NO3)2,混合溶液进行了如图实验,对溶液A和固体B的成分进行了分析和实验探究.
某化学小组用一定量AgNO3和Cu(NO3)2,混合溶液进行了如图实验,对溶液A和固体B的成分进行了分析和实验探究.| 实验步骤 | 现 象 | 有关反应的化学方程式 |
| 取少量固体B,滴加 | 有气泡产生 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
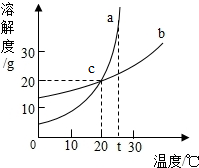 如图是a、b两种固体物质的溶解度曲线,试回答:
如图是a、b两种固体物质的溶解度曲线,试回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com