
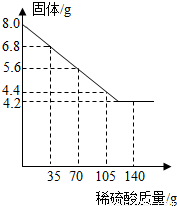
 为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成.某同学进行了如下实验:称量8.0g该混合物粉末放入烧杯中→将140g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图.试计算:
为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成.某同学进行了如下实验:称量8.0g该混合物粉末放入烧杯中→将140g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图.试计算: =
= m=24,所以金属为镁;
m=24,所以金属为镁; x=0.3g
x=0.3g

科目:初中化学 来源: 题型:
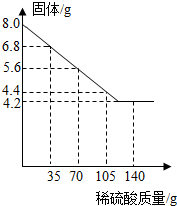 为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成.某同学进行了如下实验:称量8.0g该混合物粉末放入烧杯中→将140g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图.试计算:
为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成.某同学进行了如下实验:称量8.0g该混合物粉末放入烧杯中→将140g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图.试计算:查看答案和解析>>
科目:初中化学 来源:北京模拟题 题型:计算题

查看答案和解析>>
科目:初中化学 来源:2011年北京市中考化学预测试卷(A)(解析版) 题型:解答题
 (2012?北京二模)为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成.某同学进行了如下实验:称量8.0g该混合物粉末放入烧杯中→将140g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图.试计算:
(2012?北京二模)为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成.某同学进行了如下实验:称量8.0g该混合物粉末放入烧杯中→将140g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图.试计算:查看答案和解析>>
科目:初中化学 来源:2011年江苏省连云港市赣榆县赣马二中中考化学模拟试卷(解析版) 题型:解答题
 (2012?北京二模)为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成.某同学进行了如下实验:称量8.0g该混合物粉末放入烧杯中→将140g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图.试计算:
(2012?北京二模)为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成.某同学进行了如下实验:称量8.0g该混合物粉末放入烧杯中→将140g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图.试计算:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com