


科目:初中化学 来源: 题型:阅读理解
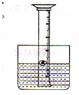 15、某化学课外兴趣小组,开展了以下两项活动:
15、某化学课外兴趣小组,开展了以下两项活动: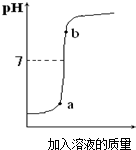 实验过程中溶液的pH变化曲线如右图所示:
实验过程中溶液的pH变化曲线如右图所示:查看答案和解析>>
科目:初中化学 来源: 题型:
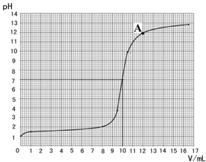 实验室需配制4%的氢氧化钠溶液200g,并用此溶液测定某敞口放置一段时间的盐酸的溶质质量分数.
实验室需配制4%的氢氧化钠溶液200g,并用此溶液测定某敞口放置一段时间的盐酸的溶质质量分数.| 加入氢氧化钠 的体积/mL |
0 | 1.0 | 8.0 | 9.5 | 10.5 | 12.0 | 16.5 |
| 烧杯中溶液pH | 1.0 | 1.3 | 2.0 | 3.9 | 9.9 | 11.9 | 12.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
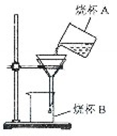
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com