
(3分)根据元素周期表的部分信息,回答下列问题:
| 1 H 氢 | | | | | | | | 2 He 氦 |
| 3 Li 锂 | 4 Be 铍 | | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 |
| 11 Na 钠 | 12 Mg 镁 | | 13 Al 铝 | 14 Si 硅 | 15 P 磷 | 16 S 硫 | 17 Cl 氯 | 18 Ar 氩 |
(1)Al2O3 (2)金属元素→非金属元素→稀有气体元素(合理即可) (3)A
解析试题分析:(1)原子序数为8、13号的元素分别是O、Al,已知Al的化合价为+3价,O的化合价为-2价,根据“正价在左,负价在右”的书写规则,结合化合价的原则,“在化合物中,正负化合价的代数和为零”,可知氧化铝的化学式为Al2O3。
(2)根据元素周期表可知,同一横行元素的排列规律是从左至右:原子序数(核电荷数)依次增大。
(3)根据元素的概念分析,元素是具有相同核电荷数或质子数的一类原子的总称,故表中不同种元素最本质的区别是质子数不同,故选A。
考点:元素周期表的特点及其应用,化学式的书写及意义,化合价规律和原则
点评:解答本题的关键是要理解和熟练掌握化学式的写法,理解元素周期表的特点,并能在解题中灵活应用。


科目:初中化学 来源: 题型:
| 族 周期 |
ⅠA | 0 | ||||||
| 1 | 1H 氢 1.008 |
ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | 6C 碳 12.01 |
7N 氮 14.01 |
8O 氧 16.00 |
9F 氟 19.00 |
||||
| 3 | 11Na 钠 22.99 |
12Mg 镁 24.31 |
铝 | |||||
 ,其中x为
,其中x为查看答案和解析>>
科目:初中化学 来源: 题型:
(7分)
元素周期表是学习和研究化学的重要工具。试根据提供的元素周期表回答问题:
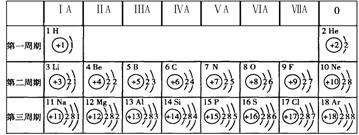
从上图中,我发现如下规律:
(1)在化学反应中,ⅠA族元素(除H外)的原子比较容易 电子,ⅥA族元素的原子比较容易 电子,都通常达到8个电子的稳定结构,可见元素的化学性质主要决定于原子的 数。
(2)从原子结构方面看:同一周期的元素具有相同的数;同一族的元素具有相同的 数。
(3)原子序数与元素原子的 数在数值上相等;
(4)
查看答案和解析>>
科目:初中化学 来源: 题型:
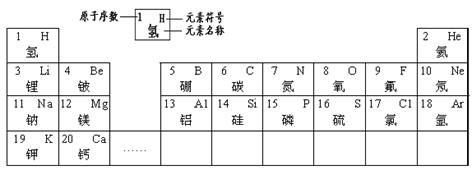
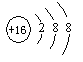 如左图的结构示意图表示的是 (写粒子符号)。
如左图的结构示意图表示的是 (写粒子符号)。
查看答案和解析>>
科目:初中化学 来源:2011-2012学年江苏省九年级上学期期末模拟考试化学试卷 题型:填空题
(7分)元素周期律和周期表是研究化学的重要工具。下表是元素周期表的部分信息。

请认真分析表中信息,回答下列问题。
(1)从原子结构看, Na和Mg同属于第三周期的原因是 ,F和Cl属于同一个族的原因是 。
(2)从元素种类看,每一周期从左到右由 元素过渡到 元素,并以稀有气体元素结束。
(3)由8和13号两种元素组成的化合物是 (写化学式)。
(4) 如左图的结构示意图表示的是 (写粒子符号)。
如左图的结构示意图表示的是 (写粒子符号)。
(5)根据下表中相关信息,判断出的元素名称不一定合理的是 (选填序号)。

查看答案和解析>>
科目:初中化学 来源:2011-2012学年北京市东城区九年级上学期期末考试化学试卷 题型:填空题
(6分)元素周期表是学习化学的重要工具,下表是元素周期表的一部分。请回答下列问题:
|
1 H |
|
2 He |
|||||
|
3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne |
|
11 Na |
12 Mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar |
(1)元素周期表中不同种元素最本质的区别是 (填序号)。
A.相对原子质量不同
B.质子数不同
C.中子数不同
(2)镁元素的原子结构示意图为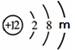 , 则m = ,该原子在化学反应中易
, 则m = ,该原子在化学反应中易
(填“得到”或“失去”)电子。说明元素的化学性质与原子的 关系密切。
(3)元素周期表中每一个横行叫做一个周期。以第二周期为例,根据图-6该周期中各元素的原子结构示意图,分析同一周期元素之间的排列有一定的规律,如: (填序号)。
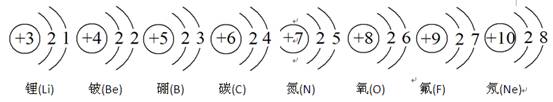
A.从左到右,各元素原子的电子层数相同
B.从左到右,各元素的原子序数依次递增
C.从左到右,各元素原子的最外层电子数相同
(4)由1号和8号元素组成的化合物(分子中原子个数比为2:1)与6号元素的单质,在高温下发生置换反应,生成一种最轻的气体和一种由双原子分子构成的化合物,该反应的化学方程式是__ __。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com