


 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案科目:初中化学 来源: 题型:
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | --- |
| 熔点/℃ | --- | --- | 1535 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
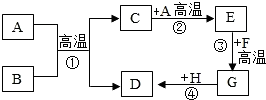 A-H都是初中化学常见的物质,它们的转化关系如图所示.A、B均为黑色粉末;D、F均为红色固体,且D为单质;C能使澄清石灰水变浑浊.请回答:
A-H都是初中化学常见的物质,它们的转化关系如图所示.A、B均为黑色粉末;D、F均为红色固体,且D为单质;C能使澄清石灰水变浑浊.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com