

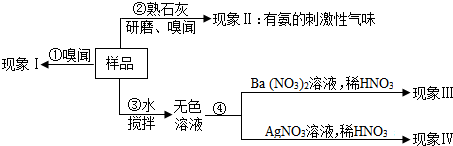
| ¼ŁÉčŗĶĻÖĻó | ÅŠ¶ĻŗĶ»Æѧ·½³ĢŹ½ | a | ČōĻÖĻóIĪŖĪŽ°±Ī¶£® | Ōņѳʷ֊²»ŗ¬ Ģ¼ĖįĒāļ§ Ģ¼ĖįĒāļ§ £ØĢīĆū³Ę£©£® |
b | ÓɲŁ×÷¢ŚĻÖĻóÅŠ¶Ļ£® | øĆѳʷŅ»¶Øŗ¬ÓŠ ļ§øł ļ§øł Ąė×Ó£® |
c | ČōĻÖĻó¢óĪŖ°×É«³Įµķ£¬ĻÖĻó¢ōĪŖĪŽ³Įµķ£® | Ōņѳʷ֊ŗ¬ÓŠ ĮņĖįļ§ ĮņĖįļ§ £ØŠ“Ćū³Ę£©£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ØNH4£©2SO4+Ba£ØNO3£©2=BaSO4”ż+2NH4NO3 £ØNH4£©2SO4+Ba£ØNO3£©2=BaSO4”ż+2NH4NO3 £® |
d | ČōĻÖĻó¢óĪŖ”°ĪŽ³Įµķ”±£¬ĻÖĻó¢ōĪŖ°×É«³Įµķ£® | Ōņѳʷ֊ŗ¬ÓŠ NH4Cl NH4Cl £ØŠ“»ÆѧŹ½£©£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖNH4Cl+AgNO3=AgCl”ż+NH4NO3 NH4Cl+AgNO3=AgCl”ż+NH4NO3 £® |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ČÜÖŹ | µā | øßĆĢĖį¼Ų | |||
| ČܼĮ | Ė® | ĘūÓĶ | ¾Ę¾« | Ė® | ĘūÓĶ |
| ČܽāŠŌ | ²»ČÜ | Ņ×ČÜ | æÉČÜ | Ņ×ČÜ | ²»ČÜ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
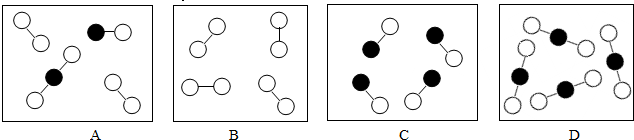
| ||
| ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
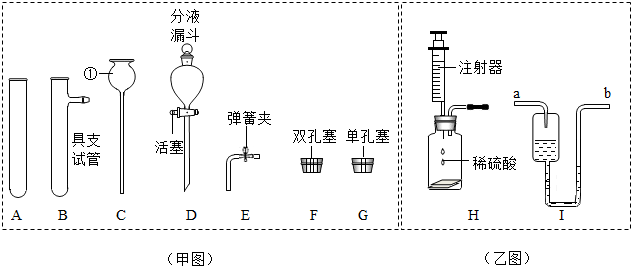
| ||
| ”÷ |
| ||
| ”÷ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ||
| ĪļÖŹ | ŅŅ“¼ | ŃõĘų | ¶žŃõ»ÆĢ¼ | Ė® | Ņ»Ńõ»ÆĢ¼ |
| ·“Ó¦Ē°ÖŹĮæ£Øg£© | 4.6 | 8.8 | 0 | 0 | 0 |
| ·“Ó¦ŗóÖŹĮæ£Øg£© | 0 | 0 | 6.6 | 5.4 | a |
| ||
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com