

分析 (1)根据地壳中各元素含量的排序及元素的分类进行分析判断.
(2)根据金属的性质分析;
(3)根据铁生锈的条件和防锈方法,进行分析;
(4)根据金属与酸能否反应以及反应的剧烈程度可以比较金属的活动性的强弱;
(5)根据金属与盐反应的原理及生成物考虑本题;
解答 解:(1)地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,其中含量最多的金属元素是铝元素.故答案为:Al;
(2)金属具有良好的导电性,常用来作导线,故答案为:C;
(3)铁生锈的条件是:铁与空气和水直接接触,根据铁生锈的条件,请说出一个铁制品采取的防锈措施油漆.故答案为:水,油漆等;
(4)将锌、铜、铁三种金属分别投入到足量的稀硫酸中,锌反应最快,反应较慢是铁,铜不能反应,故表现出三种不同的现象,原因是三种金属的活动性不同,故答案为:金属活动性不同;
(5)铁粉能与Cu(NO3)2和AgNO3反应,从而置换出Cu和Ag;向滤渣中加入少量稀盐酸,无气体产生,说明铁粉完全反应掉,由于Ag的活动性比Cu弱,所以铁先与AgNO3反应,如果铁粉的量不足,只能置换出全部或部分Ag;如果铁粉的量较足,可能置换出全面的Ag后,再置换出部分Cu;故答案为:Ag或Ag和Cu.
故答案为:
(1)Al;(2)C;(3)水; 油漆等合理即可;(4)金属活动性不同;(5)Ag或Ag和Cu.
点评 熟记地壳里各元素的含量,掌握金属的性质以及金属的活动性顺序和金属与盐的反应是解答问题的关键.


科目:初中化学 来源: 题型:解答题
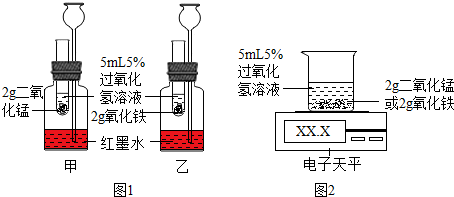
| 实验步骤 | 实验现象 | |
| 实验1 | 在试管中加入少量的H2O2溶液,然后将带火星的木条伸入试管中,观察现象. | 木条不复燃 |
| 实验2 | 在实验1的试管中加入ag的氧化铁,然后将带火星的木条伸入试管中,观察现象. | 木条复燃 |
| 实验3 | 待实验2试管中没有气泡产生后,再加入过氧化氢溶液,然后将带火星的木条伸入试管中,观察现象.反复多次实验. | 木条均复燃 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲-②,乙-③ | B. | 乙-③,丙-① | C. | 丙-①,丁-② | D. | 丁-①,丙-③ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
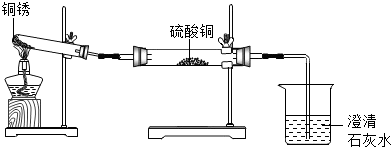
| 实验橾作 | 实验现象 | 实验结论 |
| ①按如图组装仪器,装入药品. ②加热铜锈,直至不再有气体产生,停止加热. | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊. | 加热铜锈生成的物质有 CO2、H2O、CuO;铜绣由Cu、C、H、O元素组成;烧杯中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O. |
| ③冷却后,向试管中固体 加入适量稀硫酸,稍加热. | 黑色固体溶解,溶液变 为蓝色. |
| 序号 | 实验内容 | 实验结论 | 实验反思 |
| 实验1 |  | 在干燥环境中,铜不易生锈 | (1)实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其原因是 除去蒸馏水中溶解的O2和CO2. (2)如果要证明铜生锈的快慢是否与二氧化碳的浓度有关,还需要补充的一个实验内容是 按实验4内容重复操作后,再通入一定量的CO2排出部分空气,塞紧胶塞. |
| 实验2 | 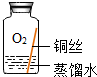 | 在有O2和H2O、无CO2的环境中,铜不易生锈 | |
| 实验3 |  | 在有CO2和H2O、无O2的环境中,铜不易生锈 | |
| 实验4 | 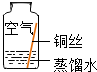 | 铜生锈的条件是 与O2、CO2和H2O同时接触 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧气的化学性质比较活泼,属于可燃物 | |
| B. | 氮气的化学性质不活泼,可用于食品防腐 | |
| C. | 空气质量报告中所列的空气质量级别越大,空气质量越好 | |
| D. | 二氧化碳在空气中含量增多会引起温室效应,属于空气污染物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①③⑥ | B. | ①③④ | C. | ①②④ | D. | ②⑤⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | B. | 2Al+3H2SO4═Al2(SO4)3+3H2↑ | ||
| C. | 2H2O═2H2+O2 | D. | Fe+O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com