
分析 (1)根据化石燃料的分类进行分析;
(2)根据二氧化碳在光照、催化剂条件下反应生成氧气和一氧化碳写出反应的化学方程式即可;
(3)根据化学方程式进行计算即可.
解答 解:(1)常见的化石燃料包括煤、石油和天然气.
(2)二氧化碳在光照、催化剂条件下反应生成氧气和一氧化碳,反应的化学方程式为:2CO2$\frac{\underline{\;\;\;光照\;\;\;}}{催化剂}$2CO+O2;
(3)二氧化碳在光照、催化剂条件下反应生成氧气和一氧化碳,反应的化学方程式为:2CO2$\frac{\underline{\;\;\;光照\;\;\;}}{催化剂}$2CO+O2.设吸收2.2kg 二氧化碳时,产生一氧化碳的质量为X,则:
2CO2$\frac{\underline{\;\;\;光照\;\;\;}}{催化剂}$2CO+O2
88 56
2.2kg X
$\frac{88}{2.2kg}=\frac{56}{X}$
X=1.4kg
答:吸收2.2kg 二氧化碳时,产生一氧化碳的质量为1.4kg;
故答案为:(1)天然气;(2)2CO2$\frac{\underline{\;\;\;光照\;\;\;}}{催化剂}$2CO+O2;(3)1.4.
点评 本题难度不大,主要考查化石燃料的分类、根据反应原理书写化学方程式的能力和根据化学方程式进行计算的能力.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 三氧化二铝为氧化物 | |
| B. | 该反应为置换反应 | |
| C. | 该反应中各元素的化合价均未发生变化 | |
| D. | 该反应放出大量的热 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 有石油的地方一般都有天然气 | |
| B. | 爱护水资源一方面要节约用水,另一方面要防治水体污染 | |
| C. | 稀有气体约占空气总体积的0.94% | |
| D. | 人类使用最广泛的金属是铝 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤液中不含Cu 2+ | B. | 金属活动性:Fe>Cu | ||
| C. | 滤渣含有铁和铜 | D. | 滤液质量比原溶液质量大 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 春蚕到死丝方尽,蜡炬成灰泪始干 | B. | 炮竹声中一岁除,春风送暖入屠苏 | ||
| C. | 千锤万凿出深山,烈火焚烧若等闲 | D. | 不知近水花先发,疑是经冬雪未销 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 改进汽车尾气净化技术 | B. | 开发新能源代替化石燃料 | ||
| C. | 植树、造林、种草 | D. | 节假日燃放烟花爆竹 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铝、钡、钛是人体非必需的微量元素 | |
| B. | 患甲状腺肿大,要多补充些含碘的食物 | |
| C. | 人体缺氟元素,会得骨质疏松病 | |
| D. | 缺乏维生素A会引起坏血病 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
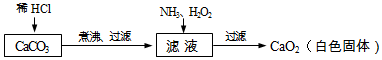
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com