
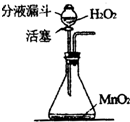
 �������⣨��ѧʽΪH2O2���׳�˫��ˮ���ڳ�������һ����ɫҺ�壬���ڶ������̣�MnO2����������Ѹ�ٷֽ⣬�ų�������ͬʱ����ˮ����ʵ�����п�����ͼ��ʾװ����˫��ˮ��ȡ������ͨ����Һ©�����������ġ����������ء�������ʱ����ƿ�еμ�˫��ˮ���������ʵ�������ô˷���������ȸ����������ȡ�����������������Щ�ŵ㣿
�������⣨��ѧʽΪH2O2���׳�˫��ˮ���ڳ�������һ����ɫҺ�壬���ڶ������̣�MnO2����������Ѹ�ٷֽ⣬�ų�������ͬʱ����ˮ����ʵ�����п�����ͼ��ʾװ����˫��ˮ��ȡ������ͨ����Һ©�����������ġ����������ء�������ʱ����ƿ�еμ�˫��ˮ���������ʵ�������ô˷���������ȸ����������ȡ�����������������Щ�ŵ㣿


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ư����Ч�ɷݴ������ƣ�NaClO���У���Ԫ��Ϊ+l�� | ||
B����������ṹʽ��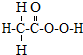 ���仯ѧʽΪ��C2H4O3 ���仯ѧʽΪ��C2H4O3 | ||
C���������⣨
| ||
| D����ʯ�ҵĻ�ѧʽ��CaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ʵ���ҳ�����ȡ�����ķ����У�a����������غͶ������̷�ĩ�� b�����ȸ�����ع��壻c���ö������̷�ĩ������ʹ�������⣨H2O2����Һ�ֽ������������ʵ��װ����ͼ��ʾ��
ʵ���ҳ�����ȡ�����ķ����У�a����������غͶ������̷�ĩ�� b�����ȸ�����ع��壻c���ö������̷�ĩ������ʹ�������⣨H2O2����Һ�ֽ������������ʵ��װ����ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����Ϊ���л�ѧ�������ʣ���H��C��O��Cl��Na��Ca��Cu��Fe�е�Ԫ����ɣ�
����Ϊ���л�ѧ�������ʣ���H��C��O��Cl��Na��Ca��Cu��Fe�е�Ԫ����ɣ��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com