
将等质量的镁、铁、锌,分别放入三份溶质质量分数相同的稀盐酸中,反应生成的H2质量与反应时间的关系如图所示,根据图中的信息,作出的判断不正确的是( )
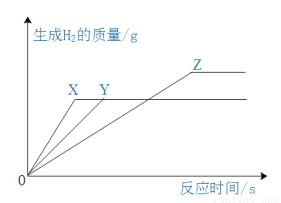
A. X、Y、Z分别表示镁、锌、铁 B. 铁消耗的盐酸质量最大
C. 镁、锌、铁过量,盐酸不足 D. 镁、锌消耗的盐酸质量相同
C 【解析】 由图可知,三种金属的活动性顺序为X>Y>Z,则金属X为镁,Y为锌,Z为铁,A正确;由图可知,铁生成的氢气质量最大,根据反应前后氢元素的质量守恒,且稀盐酸的溶质质量分数相同,可以判断铁消耗的稀盐酸质量最大,B正确;镁和锌反应生成氢气的质量相同,说明镁有剩余,锌可能反应完全,也可能有剩余,C错误;镁和锌反应生成氢气的质量相同,则消耗稀盐酸的质量是相同的,D正确。故选C。 ...科目:初中化学 来源:人教版2018届九年级上册化学:第一单元 课题1 物质的变化和性质 同步练习 题型:单选题
物质的性质与用途密切相关。 下列做法不合理的是
A. 工业上用稀盐酸除铁锈
B. 农业上用熟石灰改良酸性土壤
C. 碳酸钠用于玻璃、 造纸、 洗涤剂的生产
D. 水壶中的水垢(主要成分是碳酸钙和氢氧化镁) 用水清洗
D 【解析】 A.铁锈 的主要成分是氧化铁,能和盐酸反应生成可溶的物质,工业上用稀盐酸除铁锈;B.氢氧化钙能和酸发生中和反应,农业上用熟石灰改良酸性土壤;C.碳酸钠用于玻璃、 造纸、 洗涤剂的生产;D.水垢的主要成分是碳酸钙和氢氧化镁,都不溶于水,不用水清洗,都能与酸反应生成易溶于水的物质,应用酸清洗。选D查看答案和解析>>
科目:初中化学 来源:北京市丰台区2018届九年级5月统一测试(一模)化学试卷 题型:简答题
阅读下面科普短文。
酸奶是以新鲜的牛奶为原料,经过杀菌后再向牛奶中添加有益菌,发酵后,再冷却灌装的一种牛奶制品。酸奶不但保留了牛奶的营养,而且某些方面更优于牛奶。
酸奶比牛奶更容易被人体消化吸收,因为在发酵过程中,牛奶中约20%的糖、蛋白质被分解成为小分子,同时产生人体所必需的多种维生素。发酵后产生的乳酸可有效提高钙、磷在人体中的吸收。
酸奶中含有大量乳酸菌,乳酸菌把乳糖转化成乳酸,使得牛奶的酸度升高。酸度可以影响酸奶的口感和营养。研究者选取某种市面常见的酸奶进行实验,数据如下图所示:

酸奶喝得过多会导致胃酸过多,影响胃黏膜及消化酶的分泌,对于健康的人来说,每天250克左右是比较合适的。而且最好不要在空腹时喝含有乳酸菌的酸奶,一般选择饭后喝效果比较好。
近年来,常温酸奶逐渐流行起来。常温酸奶和低温酸奶的加工工艺不同。低温酸奶仅在生牛乳状态时经过一道灭菌处理,乳酸菌可以存活其中,但保存条件苛刻,需低温存储,且保质期较短。而常温酸奶需要进行“巴氏灭菌热处理”,该处理方式会杀灭一切细菌,所以可以常温保存较长时间。
酸奶营养美味,建议在购买的时候,仔细看配料表,根据需求去选择。
依据文章内容回答下列问题。
(1)新鲜牛奶制作酸奶的过程属于_________变化(填“物理”或“化学”)。
(2)酸奶是补钙佳品,这里的“钙”指的是_________(填字母序号)。
A.钙元素 B.钙原子 C.钙单质
(3)酸奶中的蛋白质更易消化和吸收,原因是____________。
(4)由图中数据可知,影响酸奶酸度的因素有____________。
(5)下列说法中,不合理的是____________(填字母序号)。
A.酸奶营养丰富,但要注意适量饮用
B.酸奶适宜在饭前饮用
C.常温酸奶中含有丰富乳酸菌
D.酸奶更有利于人体对钙的吸收
化学A 发酵过程中约20%的糖、蛋白质被分解成为小分子时间、温度B 【解析】 (1)由题文可知,鲜奶生产酸奶的过程中有新物质生成,故是化学变化; (2)补钙物质中的钙不是以分子、原子或单质的形式存在,是指钙元素,故选A; (3)酸奶在发酵过程中约20%的糖、蛋白质被分解成为小分子,更易消化和吸收; (4)由图可知温度越高,酸碱度越高,时间越长,酸碱度越高,故与时间和温...查看答案和解析>>
科目:初中化学 来源:江西省上饶市广丰区2018届九年级(5月份)中考模拟化学试卷 题型:实验题
将一段去除氧化镁的镁条放入一定量的盐酸中,有气泡产生,充分反应后静置,发现试管中有白色沉淀产生。为探究白色沉淀的成分,9 (1)班兴趣小组同学在老师的指导下进行如下实验:
试管(盛有等体积等浓度的盐酸) | ① | ② | ③ | ④ |
镁条质量(g) | 1 | 1.5 | 2 | 2.5 |
实验现象 | 快速反应,试管发热,镁条全部消失 | |||
白色沉淀量(恢复至20℃) | 无 | 少量 | 较多 | 很多 |
(1)4支试管中盛有等体积等浓度的盐酸的原因________________。
(得出结论)(2)镁条与盐酸反应产生白色沉淀的量与________________有关。
(提出问题)白色沉淀是什么物质?
(查阅资料)在氯化镁溶液中,镁能与水常温下反应生成氢氧化镁和氢气。
(猜想与假设)
甲:白色沉淀可能是碳酸镁
乙:白色沉淀可能是生成的氯化镁增多析出的晶体
丙:白色沉淀可能是剩余的镁
丁:白色沉淀可能是氢氧化镁
(3)其他同学认为甲的猜想是错误的,原因是________________
(实验验证)
序号 | 操作步骤 | 实验现象 | 结论 |
1 | 取第一份白色不溶物于试管中,加入蒸馏水,震荡 | (4)沉淀________________溶解(选填会或不会) | 乙同学猜想不成立 |
2 | 取第二份白色不溶物于试管中,加入稀盐酸 | (5)________________ | 丙同学猜想不成立 |
3 | ①取第三份白色不溶物于试管中,加入稀硝酸 ②向所得溶液加入几滴硝酸银溶液 | ①白色沉淀不溶解 ②出现大量白色沉淀 | ①丁同学猜想不成立 ②白色不溶物一定含(6)________________元素 |
(7)在老师的帮助下,同学们得出白色沉淀物是Mg2(OH)2Cl2反应的化学方程式为2Mg+2HCl+2H2O=Mg2(OH)2Cl2+2X则X为________________。
(拓展延伸)
小钢同学认为上述实验验证3的设计不严密,在实验验证3之前应该对不溶物进行洗涤,目的是________________。
便于对比。镁条质量。反应物中不含有碳元素,不可能生成碳酸镁。不会不产生气泡白色不溶物一定含氯元素H2。排除氯离子的干扰。 【解析】 (1)用控制变量法做探究实验时,要保证其他因素相同,只留一个变量,这样才便于对比,得出准确的结论。(2)由表格数据可知,在盐酸的体积和浓度相同的条件下,镁条质量越大,产生白色沉淀的量越多。(3)根据质量守恒定律可知,反应前没有碳元素,反应后就得不到碳酸镁。...查看答案和解析>>
科目:初中化学 来源:江西省上饶市广丰区2018届九年级(5月份)中考模拟化学试卷 题型:选择填充题
下列实验方案合理的是______
选项 | 实验目的 | 所用试剂或方法 |
A | 鉴别热塑性塑料和热固性塑料 | 加热,观察外形变化 |
B | 鉴别磷矿粉、氯化铵、氯化钾 | 观察颜色,加水 |
C | 除去硝酸钾中少量的氯化钠 | 溶解、过滤 |
D | 鉴别腈纶和纯羊毛衫 | _______________ |
查看答案和解析>>
科目:初中化学 来源:江西省上饶市广丰区2018届九年级(5月份)中考模拟化学试卷 题型:单选题
点燃某物质后,在火焰的上方罩一个干燥的烧杯,烧杯内壁有水珠出现,将烧杯倒过来,倒入澄清石灰水,振荡,石灰水变浑浊,原物质可能是( )
A. 氢气 B. 碳 C. 一氧化碳 D. 甲烷
D 【解析】 烧杯内壁有水珠出现,说明生成物有水;澄清石灰水变浑浊,说明生成物有二氧化碳。根据质量守恒定律,原物质中一定含有碳元素和氢元素,可能含有氧元素。氢气中只含有氢元素,氢气燃烧能生成水,但不能生成二氧化碳,A错误;碳中只含有碳元素,碳燃烧能生成二氧化碳,不能生成水,B错误;一氧化碳中含有碳元素和氧元素,一氧化碳燃烧能生成二氧化碳,不能生成水,C错误;甲烷中含有碳元素和氢元素,燃...查看答案和解析>>
科目:初中化学 来源:江苏省苏州市2018届九年级中考二模考试化学试卷 题型:综合题
请结合下图回答问题。
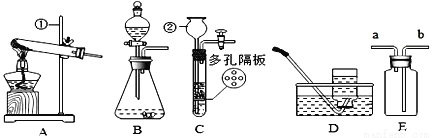
(1)仪器②的名称:____________。
(2)用氯酸钾和二氧化锰制取氧气,可选用装置____________(选填序号)和装置D组合,反应的化学方程式为____________,二氧化锰的作用是____________,若用B和D组合制取氧气,其反应的化学方程式为_____。
(3)实验室可用装置B或C制H2,C装置相对于B的优点有______,用E装置收集H2,气体应从______(选填“a”或“b”)端通入。
(4)某些大理石中含少量硫化物,使制得的CO2中混有H2S等气体。欲获取纯净、干燥的CO2,设计实验如下:
查阅资料:I.H2S能与NaOH、CuSO4等物质反应。
Ⅱ.CO2中混有的HC1气体可用饱和NaHCO3溶液吸收。

①装置甲中所盛试剂应选用____________(填字母)。
a.浓硫酸 b.NaOH溶液 c.澄清石灰水 d.CuSO4溶液
②装置丙的作用是____________。
长颈漏斗A2KClO32KCl+3O2↑催化2H2O22H2O+O2↑能够控制反应的进行与停止ad干燥CO2或除去水蒸气 【解析】 根据所学知识和题中信息知,(1)仪器②的名称:长颈漏斗。(2)用氯酸钾和二氧化锰制取氧气,可选用装置A和装置D组合,反应物是固体需加热制取气体,氧气不易溶于水,可以用排水法收集,二氧化锰的作用是催化作用,若用B和D组合制取氧气,反应物是液体和固体不需加热制...查看答案和解析>>
科目:初中化学 来源:江苏省苏州市2018届九年级中考二模考试化学试卷 题型:单选题
下列指定反应的化学方程式正确的是 ( )
A. 酸雨的形成原理:CO2 + H2O=H2CO3
B. 利用赤铁矿炼铁:Fe3O4+4CO 3Fe+4CO2
3Fe+4CO2
C. 不能用铁制容器配制波尔多液:2Fe + 3CuSO4 = Fe2(SO4)3 + 3Cu
D. 铜绿的形成:2Cu+O2+H2O+CO2 =Cu2(OH)2CO3
D 【解析】A、酸雨的形成原理是二氧化硫与水反应生成亚硫酸,正确的化学方程式应为SO2+H2O=H2SO3,错误;B、赤铁矿的主要成分是Fe2O3不是Fe3O4,利用赤铁矿炼铁,在高温下CO和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO 2Fe+3CO2,错误;C、铁与硫酸铜溶液反应生成硫酸亚铁溶液和铜,正确的化学方程式应为:Fe+CuSO4═FeSO4+Cu,错误;D、...查看答案和解析>>
科目:初中化学 来源:山东省2018届九年级学生素质教育特长展示测评化学试卷 题型:综合题
(1)汽车尾气中含有CO和NO等有害物质,可在汽车尾部安装一个催化转换器,将其转换成为无害物质。在用铂、钯作催化剂的条件下,使CO与NO反应生成绿色植物光合作用所需的一种气体和空气中体积分数最大的一种气体。试写出有关反应的化学方程式________,该反应中,_______元素的化合价升高,则该元素的原子____(填“得到”或“失去”)电子,则该元素的原子被________(填“氧化”或“还原”)。该反应中氧化剂是_____,氧化产物是______。(填化学式)
(2)某固态混合物中含有mgKNO3和若干克不溶于水的杂质,将此混合物加入ng水中,在10℃,40℃,75℃时观察,充分溶解后的结果如表所示。KNO3的溶解度曲线见图

通过计算回答:
①m=_______________________,n=_________________________。
②75℃时所得KNO3溶液_______(填“是”或“不是”)饱和溶液。
③若要在ng水中恰好溶解mg硝酸钾达到饱和,则温度应控制在_______。
2CO+2NO 2CO2+N2 ;C失去氧化NOCO2220.4200不是60 ℃ 【解析】 (1)根据题意,先找出反应物、生成物和反应条件,再根据化学方程式的书写步骤和要求写出反应的方程式;(2)对比温度从10℃升至40℃再升温至75℃时,硝酸钾溶解度的改变及实验中未溶固体质量的改变,由二者的关系可得出m、n的值;判断实验中75℃时还有82g未溶解固体的成分,可判断此时所得KNO3溶...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com