
分析 根据质量守恒定律可知,海水中的镁元素最后转化成了氢氧化镁沉淀,求出氢氧化镁沉淀中的镁元素质量就是海水中的镁元素质量,然后求出质量分数.
解答 解:氢氧化镁(Mg(OH)2)的相对分子质量为:24+(16+1)×2=58,所以氢氧化镁中镁的质量分数为:$\frac{24}{58}$×100%,
所以镁元素的质量为:0.29Kg×$\frac{24}{58}$×100%=0.12Kg,
所以海水中镁元素的质量分数为:$\frac{0.12Kg}{100Kg}$×100%=0.12%.
故答案为:海水中镁元素的质量分数为0.12%.
点评 本题主要考查了质量守恒定律的应用,难度不大,需要认真理解题意.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:初中化学 来源: 题型:解答题
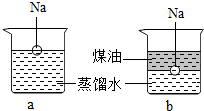 钠是一种非常活泼的金属,它能浮在水面上,与水面发生剧烈反应,反应放出的热量使钠熔化成小球,甚至会使钠和生成的氢气都发生燃烧;如图所示,把一块银白色的钠分别投入到水中和水与煤油里,在b中,钠同样与水发生剧烈反应生成氢氧化钠和氢气,但不发生燃烧.
钠是一种非常活泼的金属,它能浮在水面上,与水面发生剧烈反应,反应放出的热量使钠熔化成小球,甚至会使钠和生成的氢气都发生燃烧;如图所示,把一块银白色的钠分别投入到水中和水与煤油里,在b中,钠同样与水发生剧烈反应生成氢氧化钠和氢气,但不发生燃烧.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 500g | B. | 320g | C. | 100g | D. | 80g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
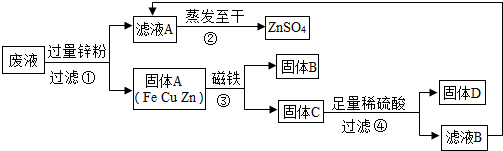
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
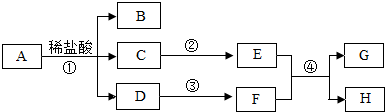
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com