
| A. | 有机物中都含有碳元素,则含有碳元素的化合物都是有机物 | |
| B. | 溶液中有晶体析出,其溶质的质量减小,则溶质的质量分数一定减小 | |
| C. | 碱性溶液能使酚酞试液变红,则滴入酚酞试液后变红的溶液一定呈碱性 | |
| D. | 碳酸盐与酸反应有气泡产生,则与酸反应有气泡产生的物质一定是碳酸盐 |
分析 A、含有碳元素的化合物叫有机化合物,简称有机物;不含碳元素的化合物是无机化合物.
B、根据有晶体析出说明是饱和溶液,根据饱和溶液的溶质的质量分数计算分析判断.
C、根据溶液的酸碱性和酸碱指示剂颜色的变化分析判断;
D、根据酸能与活泼金属、碳酸盐等反应生成气体,进行分析判断.
解答 解:A、含有碳元素的化合物叫有机化合物,简称有机物;不含碳元素的化合物是无机化合物;但含有碳元素的化合物都是有机物,碳的氧化物、碳酸盐、碳酸虽含碳元素,但其性质与无机物类似,因此把它们看作无机物,则含有碳元素的化合物不一定都是有机物,故选项推理错误.
B、当某物质一定温度下的饱和溶液在温度不变的条件下蒸发一部分溶剂后,有晶体析出,因为温度不变,物质的溶解度就不变,溶液中有晶体,剩下的溶液仍为该温度下的饱和溶液,所以溶质质量分数不变,故选项推理错误.
C、碱性溶液能使酚酞试液变红,滴入酚酞试液后变红的溶液一定呈碱性,故选项推理正确.
D、碳酸盐与盐酸反应放出气体,但与盐酸反应放出气体的物质不一定是碳酸盐,也可能是活泼金属,故选项推理错误.
故选:C.
点评 本题难度不大,掌握有机物与无机物的特征、一氧化碳和氢气的化学性质、酸的化学性质等是正确解答本题的关键.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量(g) | 4.0 | 2.0 | 3.0 | 2.0 |
| 反应后的质量(g) | 1.2 | X | 2.4 | 5.4 |
| A. | 参加反应的甲、丙质量比是1:2 | B. | 丁一定是化合物 | ||
| C. | X=2.0,乙可能是催化剂 | D. | 此反应基本类型为化合反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
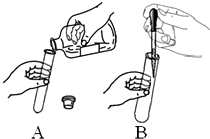 如图中是某同学验证中和反应的实验操作.A是取用稀盐酸的操作,B是向稀盐酸和酚酞的混合液中滴加NaOH溶液的示意图.
如图中是某同学验证中和反应的实验操作.A是取用稀盐酸的操作,B是向稀盐酸和酚酞的混合液中滴加NaOH溶液的示意图.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 泥水中,泥是溶质,水是溶剂 | |
| B. | 物质的溶解过程通常会伴随着能量的变化 | |
| C. | 配制溶液时,搅拌可以增大固体物质的溶解度 | |
| D. | 15℃时硝酸钾的溶解度为25g,则该温度下硝酸钾饱和溶液中溶质与溶剂的质量比为1:5 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 众所周知,在金属活动性顺序中,位于前面的金属能把位于后面的金属从其化合物的溶液中置换出来.化学小组同学将金属钠放入硫酸铜溶液时(如图),却没有得到红色的铜.
众所周知,在金属活动性顺序中,位于前面的金属能把位于后面的金属从其化合物的溶液中置换出来.化学小组同学将金属钠放入硫酸铜溶液时(如图),却没有得到红色的铜.| 实验一 | 实验操作 | 实验现象 |
| 步骤1 | 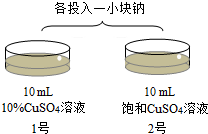 | 1号:钠在溶液中游动较少,发出嘶嘶声和持续的火光,最后消失,生成灰蓝色絮状沉淀. 2号:钠在溶液中几乎不游动,聚集在一起,发出嘶嘶声和持续的火光,最后发出啪的较大响声,然后消失,生成大量灰蓝色片状沉淀. |
| 步骤2 | 分别向1号、2号所得灰蓝色沉淀上加入等体积20%的盐酸 | 1号:沉淀完全消失,得到浅绿色溶液. 2号:沉淀完全消失,得到深绿色溶液. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com