
【题目】根据如图所示的实验,回答问题。
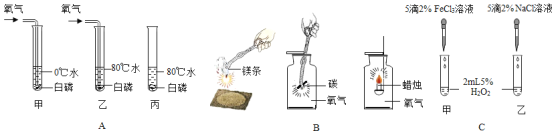
(1)A组实验中,通过对比__ 试管中的现象,可说明燃烧需要温度达到可燃物着火点。
(2)B组实验中,找出三个化学变化的一个共同点___。
(3)C组实验是探究哪种离子能促进H2O2分解的实验,现象是:甲中产生大量气泡,乙中可看到有极少量气泡出现,则加快H2O2分解的离子符号____。
【答案】甲乙 反应都放热 Fe3+
【解析】
(1)说明燃烧需要温度达到可燃物着火点,应控制其它条件相同,进行分析解答。
(2)根据氧气的化学性质,进行分析解答。
(3)根据氯化铁与氯化钠的构成,进行分析解答。
(1)说明燃烧需要温度达到可燃物着火点,应控制其它条件相同,甲乙试管中除了温度不同外,其它条件相同,故通过对比甲乙试管中的现象,可说明燃烧需要温度达到可燃物着火点。
(2)三个化学变化的共同点有反应都放热、反应物中都有氧气等。
(3)甲中产生大量气泡,乙中可看到有极少量气泡出现,氯化铁与氯化钠中均含有氯离子,则加快H2O2分解的离子是铁离子,其离子符号为Fe3+。
故答案为:
(1)甲乙;
(2)反应都放热(反应物中都有氧气等合理即可);
(3)Fe3+。


科目:初中化学 来源: 题型:
【题目】下图是元素周期表中的一部分,根据表中信息回答下列问题。
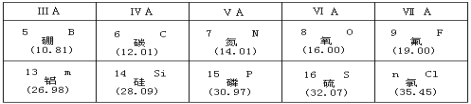
(1)用m代表的13号元素的元素符号是_____。
(2)氯元素的原子序数n等于______,它的相对原子质量是_________。
(3)氧、氟、硫、氯元素都属____(填“金属”或“非金属”)元素,它们在化学反应中一般易___(填“得”或“失”)电子,趋向于稳定结构
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质得质量如图,下列说法正确的是( )
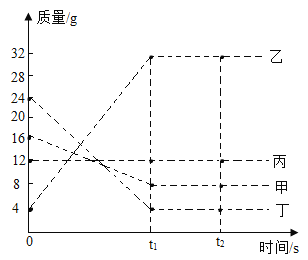
A.该反应是分解反应
B.丙一定是催化剂
C.反应中甲和丁的质量变化之比为2:5
D.反应中甲和乙的质量变化之比为2:8
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】测定水中氢、氧元素的质量比。根据下图进行实验,反应后测得甲中玻璃管(含药品)质量减少a g,乙中U形管(含药品)质量增加b g。
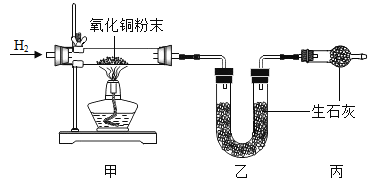
(1)水中氢、氧元素的质量比是__(用含a、b的式子表示)。
(2)下列因素中,对测定结果有影响的是____(填序号)。
A CuO粉末不干燥
B CuO没有完全转化为Cu
C 没有丙装置
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图甲、乙分别为钠元素、溴元素在元素周期表的信息,A、B、C、D为四种粒子的结构示意图,请你回答:
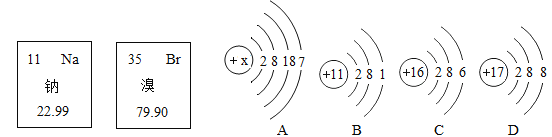
(1)若图A表示的是一种原子结构示意图,x的数值为_____。
(2)溴元素的相对原子质量_____。
(3)B、C、D中与溴元素化学性质相似的为_____。
(4)写出A、B两种原子形成化合物的化学式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧化钙和过氧化钙(CaO2)的混合物12.8g溶于足量水后,加入足量的Na2CO3溶液,溶液中的Ca2+全部转化为沉淀,过滤、干燥,得到20g CaCO3。则原12.8g混合物中钙元素与氧元素的质量之比为(已知2CaO2+2H2O===2Ca(OH)2+O2↑)( )
A. 5:2 B. 5:3 C. 5:4 D. 1:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】复分解反应存在这样一个规律:较强酸可制取较弱酸。中和反应、盐类的水解也是复分解反应,盐类的水解反应的逆反应是中和反应。盐类的水解反应中,弱酸强碱盐中弱酸根离子对应的弱酸越弱,其盐越容易发生水解。
已知在常温下测得浓度均为0.lmol/L的下列6种溶液的pH:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
pH | 8.8 | 8.1 | 11.6 | 10.3 | 11.1 | 11.3 |
(1)请根据上述信息判断下列反应不能发生的是_____(填编号)。
A ![]()
B ![]()
C ![]()
D ![]()
E ![]()
F ![]()
(2)一些复分解反应的发生还遵循其他的规律、下列变化都属于复分解反应:
①将石灰乳与纯碱溶液混合可制得苛性钠溶液
②向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打固体
③蒸发KC1和NaNO3的混合溶液,首先析出NaCl晶体。
根据上述反应,总结出复分解反应发生的另一规律为_____。
(3)已知溶液的pH与氢离子浓度有直接关系。物质的量浓度均为0.05mol/L的下列五种物质的溶液中,pH由大到小的顺序是_____(填编号)。
①C6H5OH(苯酚) ②CH3COOH ③HClO4 ④HC1O ⑤H2SO4
(4)25℃时,M酸溶液的pH=a,N碱溶液的pH=b。若X为强酸,Y为强碱,且![]() ,若两者等体积混合后,溶液的pH=7.此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是_____。
,若两者等体积混合后,溶液的pH=7.此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶液在日常生活、工农业生产和科学研究中具有广泛的用途。
(1)溶液的溶质可以是固体,也可以是_______或气体;生理盐水是医疗上常用的一种溶液,其溶质为______(填化学式)。
(2)配制溶质的质量分数为5% 的氯化钠溶液。配制步骤:①称量和量取 ②溶解 ③计算 ④装入试剂瓶贴好标签。配制上述溶液的正确顺序是_______(填序号)。
(3)如图为甲、乙两种固体物质的溶解度曲线。
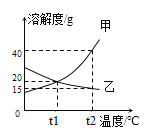
①溶解度随温度升高而增大的物质是_______(填“甲”或“乙”)。
②将t2℃时的甲、乙两种物质的饱和溶液降温至t1℃,所得溶液中溶质的质量分数甲_______乙(填“<”、“=”或“>”)。
(4)t1℃时,在50 g水中加入18 g乙固体,充分搅拌后得到______(填“饱和”或“不饱和”)溶液,升温至t2℃,此时该溶液中溶质的质量分数为______(计算结果精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如下图所示,在白色点滴板1~6的孔穴中,分别滴加稀硫酸。
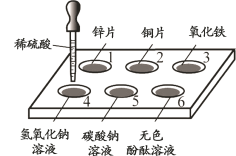
(1)反应后溶液颜色有变化的是_____(填序号)。
(2)有一个孔穴中的物质不与稀硫酸反应,原因是_____。
(3)若用石灰水替代稀硫酸滴入孔穴5中,发生反应的化学方程式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com