
分析 (1)根据该反应中只有二氧化碳是气体,则利用质量守恒定律和反应前后烧杯中物质的总质量之差来计算二氧化碳的质量;
(2)将二氧化碳的质量代入化学反应方程式来计算碳酸钙的质量;
(3)利用化学反应方程式计算出氯化钙的质量,再利用溶液的质量来计算溶质的质量分数.
解答 解:
(1)由质量守恒可知,二氧化碳的质量为22.2g+126g-139.4g=8.8g,
(2)设碳酸钙的质量为x,生成的氯化钙的质量为y,
则CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 111 44
x y 8.8g
$\frac{100}{x}=\frac{111}{y}=\frac{44}{8.8g}$
x=20g
y=22.2g
因杂质既不溶于水,也不与其他物质反应,则溶液的质量为139.4g-(22.2g-20g)=137.2g,溶质的质量为22.2g,则溶质的质量分数$\frac{22.2g}{137.2g}×$100%≈16.1%
答案:
(1)生成二氧化碳的质量8.8g
(2)石灰石中碳酸钙的质量是20g
(3)反应后所得溶液中溶质的质量分数16.1%
点评 本题考查学生利用化学反应方程式的计算,明确二氧化碳是气体并利用质量守恒来计算二氧化碳的质量是解答的关键.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀.根据如图所示的转化关系(图中反应条件均已 略去),请回答:
已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀.根据如图所示的转化关系(图中反应条件均已 略去),请回答:查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 铁锈放入稀盐酸中,溶液变浅绿色 | |
| B. | 石蕊试液滴入硫酸溶液中,溶液变红色 | |
| C. | 碳酸钠溶液中滴加氢氧化钙溶液,出现白色沉淀 | |
| D. | 硫酸铜溶液中滴加氢氧化钠溶液,出现蓝色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | X能形成化学式为X(OH)3的碱 | |
| B. | X可能形成化学式为KXO3的含氧酸钾盐 | |
| C. | X原子的最外层电子数和核电荷数肯定为奇数 | |
| D. | X能与某些金属元素形成化合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
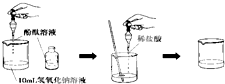 在烧杯中加入10ml氢氧化钠溶液,滴入几滴酚酞试液,再用滴管滴入稀盐酸,并不断搅拌,最终得到无色溶液.(如图所示)
在烧杯中加入10ml氢氧化钠溶液,滴入几滴酚酞试液,再用滴管滴入稀盐酸,并不断搅拌,最终得到无色溶液.(如图所示) 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com