
 和
和 分别代表两种不同的单质分子A2和B2,它们在一定条件下能发生化学反应,其反应的微观示意图如图1:
分别代表两种不同的单质分子A2和B2,它们在一定条件下能发生化学反应,其反应的微观示意图如图1: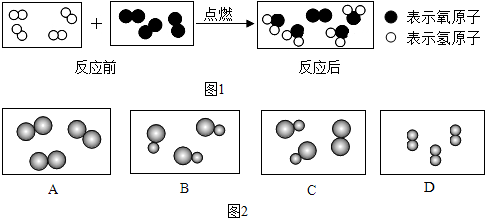
分析 (1)观察反应的微观示意图,分析反应物、生成物,写出反应的化学方程式,据其意义分析回答有关的问题;
(2)根据物质的微观构成分析物质的类别.
解答 解:(1)由反应的微观示意图可知,该反应是氢气燃烧生成水,反应的化学方程式为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
①由方程式可知,参加反应的B2与生成物分子的个数比为 1:2;
②参加反应的A2与生成物的质量之比为:4:36=1:9;
③由上述分析可知,反应的化学方程式为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
(2)由物质的微观构成可知,B物质的分子是由不同种的原子构成的,属于化合物,属于化合物,C物质是由不同种分子构成的,属于混合物.
故答为:(1)①1:2;②1:9;③2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;(2)B,C.
点评 此题是对化学反应微观示意图问题的考查,根据分子构成判断反应物与生成物的种类,依据构成相同的分子为同种物质的分子等.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:初中化学 来源: 题型:填空题
 钠的化合物在日常生活中应用广泛.
钠的化合物在日常生活中应用广泛.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 野火烧不尽,春风吹又生 | B. | 只要功夫深,铁杵磨成针 | ||
| C. | 春蚕到死丝方尽,蜡烛成灰泪始干 | D. | 爆竹声中一岁除,春风送暖入屠苏 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 实验序号 | 10%的H2O2溶液(mL) | 溶液中加入 物质(g) | 收集到气体的体积(mL) |
| 1 | 100 | 无 | a |
| 2 | 100 | Fe2O3 0.5g | b |
| 3 | 100 | MnO2 0.5g | c |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 |
| 剩余固体质量/g | 5.1 | 4.5 | 4.2 | 4.08 | 4.08 | 4.08 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
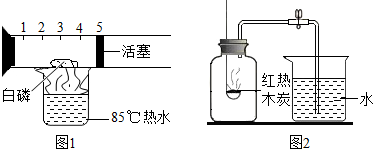
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
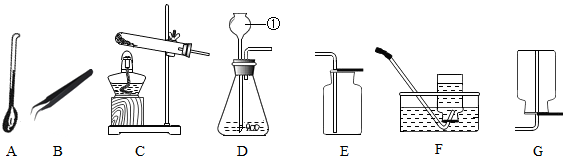
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com