
某食盐样品中含有少量沙土、氯化钙和氯化镁。以下是除去食盐样品中沙土、氯化钙和氯化镁的实验流程: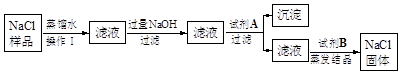
根据流程图回答:
(1)操作Ⅰ的名称是 ,加入的试剂A是 ,沉淀是 ;
(2)写出NaOH与杂质反应的化学方程式: ;
(3)加入试剂B的目的是 ;
(4)蒸发结晶时用到玻璃棒的作用是 。
(1)过滤 碳酸钠(或Na2CO3) 碳酸钙(或CaCO3)
(2)2NaOH+MgCl2 Mg(OH)2↓+2NaCl
(3)除去NaOH和Na2CO3
(4)搅拌,防止局部过热导致液滴飞溅
解析试题分析:(1)某食盐样品中含有少量沙土、氯化钙和氯化镁,沙土不溶于水,可以通过过滤,将沙土与液体分离开;加入过量氢氧化钠目的是除去杂质氯化镁,接着为了除去杂质氯化钙,且不引入新的杂质,应加入的试剂A是碳酸钠,生成的沉淀是碳酸钙;
在过滤时,除了用到玻璃棒,漏斗,还需用的玻璃仪器是烧杯,在过滤中玻璃棒的作用是引流;在蒸发结晶过程中也需要使用玻璃棒,其作用是:搅拌,防止局部过热导致液滴飞溅;
(2)加入的氢氧化钠能与杂质氯化镁反应,生成了氢氧化镁沉淀和氯化钠,反应的方程式是:2NaOH+MgCl2=Mg(OH)2↓+2NaCl;
(3)除杂加入了过量的氢氧化钠和碳酸钠,反应之后仍有剩余,因此,加入试剂B的目的是除去氢氧化钠和碳酸钠;
(4)蒸发结晶时用到玻璃棒的作用是搅拌,防止局部过热导致液滴飞溅。
考点:氯化钠与粗盐的提纯
点评:在解答本题时要注意除杂质时加入的试剂只能与杂质反应,同时不能引入新的杂质,加入的过量试剂应在后续操作中除去;将不溶于液体的固体和液体分离用过滤的方法;注意反应方程式的书写正确。


科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com