
 ��ͬ����ε�Ⱥ��ÿ��Ƶ�������������ͬ����ͼΪij����Ʒ˵�����һ���֣���ش�
��ͬ����ε�Ⱥ��ÿ��Ƶ�������������ͬ����ͼΪij����Ʒ˵�����һ���֣���ش����� �������ʵĻ�ѧʽ���Լ�����Է������������Ԫ�ص�ԭ�Ӹ����ȣ�Ҳ���Լ������Ԫ�ص�����������
̼��ƺ�ϡ���ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼�����ݷ�Ӧ�Ļ�ѧ����ʽ�����ṩ�����ݿ��Խ�����ط���ļ�����жϣ�
��� �⣺��1��ά����D3�Ļ�ѧʽΪC27H44O����ά����D3���ӵ���Է��������ǣ���12��27��+��1��44��+��16��1��=384��
����C��H��O��ԭ�Ӹ�������27��44��1��
���384��27��44��1��
��2��̼��ƣ�CaCO3���и�Ԫ�ص���������Ϊ��$\frac{40}{40+12+48}$��100%=40%��
���40%��
��3�������ɶ�����̼����Ϊx��
CaCO3+2HCl�TCaCl2+H2O+CO2����
100 44
1.5g��10 x
$\frac{100}{1.5g��10}$=$\frac{44}{x}$��
x=6.6g��
�𣺰�10Ƭ�ƶ�����������ϡ�����У��ܲ���6.6g������̼���壮
���� ������Ҫ����ѧ�����ü��跨�ͻ�ѧ����ʽ���м�����ƶϵ�����������ʱҪע��淶�Ժ�ȷ�ԣ�


 �����Ƹ���ʦ����ϵ�д�
�����Ƹ���ʦ����ϵ�д� ��ͨ����ͬ����ϰ��ϵ�д�
��ͨ����ͬ����ϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
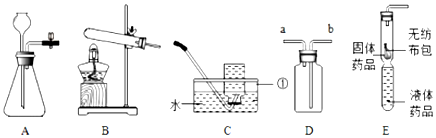
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ������������Ӻ������ӹ��ɵĴ����� | |
| B�� | �����ڲ�ͣ�˶���ԭ�Ӳ��˶� | |
| C�� | ԭ�ӵ���������������Ԫ�ص����� | |
| D�� | ���ֶ�����̼��ѧ���ʵ�������̼ԭ�Ӻ���ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
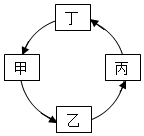 �±����и��������У�����֮�䰴��ͷ����ͨ��һ����Ӧ����ʵ����ͼ��ʾת�����ǣ�������
�±����и��������У�����֮�䰴��ͷ����ͨ��һ����Ӧ����ʵ����ͼ��ʾת�����ǣ�������| �� | �� | �� | �� | |
| A | CO2 | CaCO3 | H2O | O2 |
| B | Fe | Fe3O4 | CO | CO2 |
| C | H2O2 | H2O | O2 | MgO |
| D | CaO | Ca��OH��2 | H2O | CaCl2 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ұ������ | B�� | ������ֽ | C�� | �����մ� | D�� | ��˿֯�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ʹ����С�������� | B�� | Ͷҩɱ������ | ||
| C�� | ͨ������̿����ɫ�غ���ζ | D�� | ͨ�����˳�ȥ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������ȼ�գ������⣬�ų����������ɶ�����̼��ˮ | |
| B�� | ��˿����ʢ�����ļ���ƿ�У��������䣬���ɺ�ɫ���� | |
| C�� | ľ̿�ڿ�����ȼ�գ����ɺ�ɫ���� | |
| D�� | ����������ȼ�գ����������ɫ�����д̼�����ζ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com