
分析 根据反应可以假设两种情况分析固体的质量可能是铜,也可能是铁和铜的混合物进行计算.
解答 解:此题分两种情况:
一、假设硫酸铜过量:由于硫酸铜过量,因此铁完全反应,而且最后的剩余物只有铜,故5.2g为铜的质量,
设产生5.2g的铜需要铁的质量为x
Fe+CuSO4═FeSO4+Cu
56 64
x 5.2g
铁的质量为4.55g,因此原硫酸铜的质量就为12.8-4.55=8.25(g),则其中铜元素的质量为:8.25g×$\frac{64}{160}$×100%=3.3g,故不可能有5.2g的铜出现,因此假设不成立;
二、假设铁过量:由于铁过量,因此剩余的5.2g固体为铁和铜的混合物,
设硫酸铜的质量为x,反应铁的质量为y,生成铜的质量为z
Fe+CuSO4═FeSO4+Cu
56 160 64
y x z
$\frac{56}{y}$=$\frac{160}{x}$=$\frac{64}{z}$
y=$\frac{56x}{160}$
z=$\frac{64x}{160}$
则$\frac{56x}{160}$+$\frac{64x}{160}$=5.2g
x=8g 因此铁的质量为12.8g-8g=4.8g
故答案为:原混合物中含有硫酸铜质量为8g,铁的质量为4.8g.
点评 本题考查了金属和盐溶液的反应,难度较大,根据反应的程度分两种情况讨论计算得出结论即可.


科目:初中化学 来源: 题型:选择题
| 体液 | 唾液 | 胆汁 | 胰液 | 胃酸 |
| pH | 6.6-7.1 | 7.1-7.3 | 7.5-8.0 | 0.9-1.5 |
| A. | 唾液一定呈酸性 | B. | 胆汁一定呈碱性 | ||
| C. | 胰液能使紫色石蕊试液变红 | D. | 胃酸能使酚酞试液变红 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
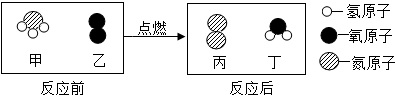
| A. | 一个甲分子中含有4个原子 | B. | 4种物质中,属于化合物的是甲和丁 | ||
| C. | 生成物丙和丁的质量比为14:27 | D. | 该反应的基本类型为复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
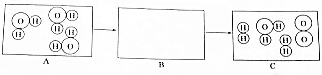
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫化羰可用来灭火 | |
| B. | 硫化羰可作为理想燃料 | |
| C. | 该反应中硫化羰、氧气、二氧化碳和二氧化硫的分子数目比为2:3:2:2 | |
| D. | 每60份质量的硫化羰与32份质量的氧气点燃完全反应,生成44份质量的二氧化碳和64份质量的二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
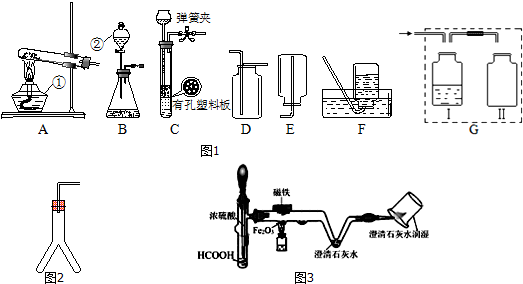
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com