
分析 (1)取用试剂后的滴管不能平放或倒置,以免药液流入胶头造成胶头腐蚀.
(2)实验剩余的药品放回原试剂瓶会造成试剂污染.
(3)加热玻璃仪器时如外壁有水,会造成试管受热不均匀.
解答 解:(1)滴管取用试剂后平放或倒置,液体试剂进入胶头而使胶头受腐蚀或将胶头里的杂质带进试液.
(2)实验剩余的药品不能放回原试剂瓶,否则会造成试剂污染.
(3)给试管加热时试管外壁有水珠,应在加热前应擦干,以防试管受热不均匀而造成试管炸裂.
故答案为:(1)液体倒流,沾污试剂或腐蚀橡胶胶帽;(2)污染试剂;(3)试管炸裂.
点评 本题难度不大,考查化学实验基本操作中出现的错误以及可能造成的后果,熟知化学实验基本操作是解答本题的关键.


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 催化剂在化学反应里只是加快化学反应速率 | |
| B. | 化合反应不一定是氧化反应,氧化反应一定是化合反应 | |
| C. | 为了防止“白色污染”,必须禁止使用一切塑料袋 | |
| D. | 给固体物质加热时,试管口要向下倾斜,目的是防止试管炸裂 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
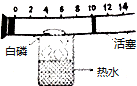 课外活动小组的同学,用如图所示的装置粗略测定空气中氧气的体积分数.该装置的气密性良好,活塞可左右滑动,实验前活塞停在刻度10cm处.已知白磷在空气中燃烧的最低温度为40℃.
课外活动小组的同学,用如图所示的装置粗略测定空气中氧气的体积分数.该装置的气密性良好,活塞可左右滑动,实验前活塞停在刻度10cm处.已知白磷在空气中燃烧的最低温度为40℃.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
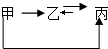
| A. | NaOH NaCl NaNO3 | B. | CO2 CaCO3 CaO | ||
| C. | CaO Ca(OH)2 CaCO3 | D. | H2O2 H2O O2 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中, 滴加氯化钡溶液(或稀盐酸). | 有白色沉淀(或有气泡) | 该溶液是碳酸钠溶液.有关反应的化学方程式为:Na2CO3+BaCl2═BaCO3↓+2NaCl(或Na2CO3+2HCl═2NaCl+H2O+CO2↑) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com