
【题目】足球比赛中让意外昏迷的球员快速恢复意识会用到“嗅盐”。同学们对“嗅盐”产生了好奇,并对其成分进行了如下探究。
(查阅资料)①嗅盐是一种盐类物质和香料(不参与下列探究中的任何反应)组成,能释放出氨味气体,对人体神经会产生强烈的刺激作用,但过量吸入会危害健康。
②氯化钙稀溶液与碳酸氢铵溶液不发生反应。 ③氨气能与硫酸化合生成硫酸铵。
(提出问题)嗅盐中盐类物质是什么?
(实验探究)填写表中空格。
实验 | 小军的实验 | 小英的实验 | |
方案 |
嗅盐与___(填一种物质)混合研磨 |
|
|
现象 | 闻到较浓烈刺激性气味且试纸变蓝 | ______ | ______ |
结论 | 嗅盐中含有NH4+ | 嗅盐中含有CO32- | 确认了小军的实验结论 |
证明嗅盐中盐类物质是碳酸铵 | |||
(质疑)小英认为小军的实验不严谨,小英通过补做一个实验(方案见上表),进而确认了小军的结论。小英的实验目的是排除嗅盐中的_______离子可能性。
(继续探究)同学们利用如图装置进一步测定嗅盐中碳酸铵的质量分数。
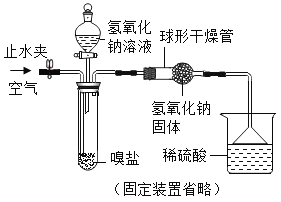
反应原理:![]() ,其中X的化学式为______。
,其中X的化学式为______。
(数据记录)实验秤取样品质量m1,反应前后装有氢氧化钠固体的球形管的总质量分别为m2和m3,反应前后烧杯及烧杯内溶液的总质量分别为m4和m5。
(数据处理)通过测得数据计算出嗅盐中碳酸铵的质量分数。
(反思与评价)关于该实验的说法正确的是______(填序号,双选)
A 嗅盐中碳酸铵的质量分数表达式为:![]()
B 倒置漏斗可以增大吸收面积同时防止倒吸
C 可以用浓硫酸代替稀硫酸
D 停止加热一段时间后要通入一段时间空气,否则测定结果会偏小
【答案】熟石灰[或Ca(OH)2等] 有气泡产生,澄清石灰水变浑浊 有白色沉淀产生 HCO3-(或碳酸氢根) Na2CO3 B、D
【解析】
碳酸铵和氢氧化钙反应生成碳酸钙和氨气和水,稀盐酸和碳酸铵反应生成氯化铵和水和二氧化碳,氯化钙和碳酸铵反应生成碳酸钙和氯化铵,二氧化碳能使澄清石灰水变浑浊。
[实验探究]
碳酸铵和氢氧化钙反应生成碳酸钙和氨气和水,稀盐酸和碳酸铵反应生成氯化铵和水和二氧化碳,氯化钙和碳酸铵反应生成碳酸钙和氯化铵,二氧化碳能使澄清石灰水变浑浊。
实验 | 小军的实验 | 小英的实验 | |
方案 |
嗅盐与熟石灰混合研磨 |
|
|
现象 | 闻到较浓烈刺激性气味且试纸变蓝 | 有气泡产生,澄清石灰水变浑浊 | 有白色沉淀产生 |
结论 | 嗅盐中含有NH4+ | 嗅盐中含有CO32- | 确认了小军的实验结论 |
证明嗅盐中盐类物质是碳酸铵 | |||
[质疑]小军的实验没有排除碳酸氢根离子的干扰。故小英的实验目的是排除嗅盐中的碳酸氢根离子可能性。
[继续探究]
反应原理为![]() ,根据质量守恒定律,反应前后原子个数相同,故X的化学式为Na2CO3。
,根据质量守恒定律,反应前后原子个数相同,故X的化学式为Na2CO3。
[反思与评价]
A、(m3-m2)质量为氢氧化钠固体质量变化值,但是本题中,生成的水不能全部被氢氧化钠吸收,且装置中氢氧化钠溶液中的水会变成蒸汽,故氢氧化钠固体改变的质量不等于生成水的质量,所以不能用X值计算碳酸铵的质量,故A不正确;
B、氨气是极易溶于水的气体,吸收氨气时要防止倒吸,倒置漏斗可以增大吸收面积同时防止倒吸,故B正确;
C、本实验是在敞开体系中进行,如果用浓硫酸代替稀硫酸,浓硫酸会吸收空气中的水分,导致测量出氨气的质量结果偏大,计算结果偏大,另浓硫酸有强烈腐蚀性,存在安全隐患,故C不正确;
D反应完成后,因为部分生成的氨气会遗留在装置中,不能被稀硫酸吸收,会导致计算结果偏小,故应该通入空气,将生成的氨气排除,保证全部的氨气被稀硫酸吸收,使计算结果更精准,故D正确。故选BD。


科目:初中化学 来源: 题型:
【题目】化学知识与应用
(1)铝制品耐腐蚀的原因是____________________________(用化学方程式表示);
(2)在牙膏中,常用轻质碳酸钙粉末作摩擦剂。人们通常用下列方法生成轻质碳酸钙:将石灰石煅烧后加水制成石灰乳,净化后与二氧化碳作用得到碳酸钙。试用化学方程式表示上述反应的原理:①___________________________________;②______________________________;③___________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“化学棋”游戏规则:①每粒棋子代表一种物质;②吃子:所选棋子能与棋盘(如图)中的某棋子发生反应,则棋盘中的该棋子被吃掉;③连吃:前一次反应的生成物能与另一棋子发生反应时,则该棋子也被吃掉。若一次就可连续吃掉棋盘上的所有棋子,应选择的棋子是
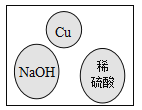
A. ![]() B.
B. ![]() C.
C. 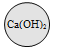 D.
D. 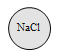
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,下列说法不正确的是( )
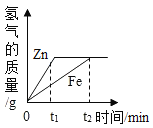
A.t1时,产生氢气的质量锌比铁大
B.t1时,产生氢气的速率锌比铁大
C.t2时,参加反应锌的质量与铁相同
D.t2时,锌、铁消耗的盐酸质量相同
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】除去食盐溶液中的Na2SO4和CaCl2杂质的操作有:①加入过量BaCl2溶液;②过滤;③加入适量盐酸;④蒸发结晶;⑤加入过量Na2CO3溶液,正确的操作顺序是( )
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸钠在生产和生活中有着广泛的用途。某校化学兴趣小组的同学们为了学习碳酸钠的化学性质,开展了如下探究活动。
[设计与实验]
同学们分别取适量的碳酸钠溶液于4支
试管中,完成如下图所示的实验。
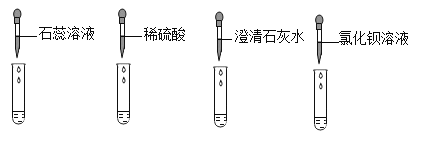
(1)实验一中,同学们观察到溶液变为蓝色。
(2)实验二中,当小婧观察到不再产生气泡时,溶液中存在的阴离子是_______(填化学符号)。
(3)实验三中,反应的化学方程式为________。
(4)实验四中,小辉看到有白色沉淀产生,该化学反应的基本类型是______。
[得出结论]
根据以上实验,兴趣小组的同学们得出了碳酸钠的化学性质,即:碳酸钠能与______反应、能与酸反应、能与某些碱反应、能与某些______反应。
[反思与提高]
(1)小亮在完成实验三时没有看到明显的实验现象,可能的原因是______。
(2)小明发现草木灰的主要成分碳酸钾在组成上与碳酸钠有相似之处,于是对草木灰的主要成分进行了检验,其实验操作、现象和结论是______。草木灰是一种常用的钾肥,对农作物的生长所起的作用是______,不能与_______混合施用。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组利用如图所示装置(图中固定装置已略去)测定铜锌合金中锌的质量分数,探究过程如下:
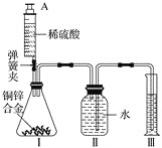
①连接实验装置并检查装置气密性。
②向装置Ⅰ中的锥形瓶加入2.0g的铜锌合金样品粉末,由注射器缓缓注入稀硫酸,待到锥形瓶中不再产生气体时,准确读取注射器内读数,减少10.5mL稀硫酸,同时立即夹紧弹簧夹,移出装置Ⅲ中的导管,准确读取量筒内水的体积为214.0mL(注:样品中的杂质不参加反应
③装置Ⅰ中剩余固体物质经过适当处理后,准确称量其质量为1.4g
④该小组的三位同学利用实验过程测得不同数据,计算铜锌合金样品中锌的质量分数
甲同学利用装置Ⅰ中反应前后固体的质量进行计算;
乙同学利用装置Ⅰ中加入稀硫酸的量进行计算;
丙同学利用装置Ⅲ中量取水的体积进行计算,并查得:在标准状况下,氢气的密度为0.09gL-1。
回答下列问题:
(1)装置Ⅰ中反应的化学方程式为___,实验过程中须加入稀硫酸至不再产生气体,目的是___。
(2)步骤③中称量剩余固体之前的正确操作是_______、洗涤、干燥。
(3)根据实验测定的数据,上述三位同学中________(填“甲”、“乙”或“丙”)同学无法进行计算样品中锌的质量分数。
(4)化学小组同学发现:按照丙同学的方案进行计算,致使实验结果出现较大偏差。以下因素可能造成偏差的有________(填标号)。
A 移出装置Ⅲ时,导管内留存了一部分水
B 实验测量前,没有排除装置Ⅰ中的空气
C 数据处理时,未排除加入稀硫酸所占的体积
【答案】(1)![]() ;使样品中的锌完全反应;(2)过滤;(3)乙;(4)AC;
;使样品中的锌完全反应;(2)过滤;(3)乙;(4)AC;
【解析】
试题(1)由于铜排在了氢的后面,所以与酸不反应,反应物是锌和硫酸,生成物是硫酸锌和氢气,氢气后面标上上升符号;实验过程中须加入稀硫酸至不再产生气体,目的是使样品中的锌完全反应;(2)从铜和硫酸锌溶液的混合物中得到铜,先进行过滤,得到带有硫酸锌溶液的铜,再进行洗涤除去表面的硫酸锌,再进行干燥除去水即可;(3)根据加入稀硫酸的量进行计算需要知道稀硫酸的溶质质量分数,而题中没有告知;(4)由于锌与硫酸反应生成硫酸锌和氢气时,放出热量,如果没等冷却到室温,根据热涨冷缩的原理可知进入量筒中水偏多,所以误认为得到的氢气多,再就是数据处理时,未排除加入稀硫酸所占的体积,计算的结果就偏大;
考点:金属的化学性质;化学方程式;实验误差分析;
点评:熟记金属活动性顺序表,知道排在氢之前的金属和稀盐酸或者硫酸反应生成氢气,而排中氢之后的金属和稀盐酸或者稀硫酸不生成氢气;化学反应中物质的质量比都是纯净物之间的质量比,而溶液中溶质的质量=溶液质量×溶质质量分数;本题容易出错的地方是对实验结果的评价,要知道锌与硫酸反应放出热量,会造成相应的误差,必须冷却到室温才能进行观察和计算。
【题型】实验题
【结束】
30
【题目】用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验设计是化学实验的重要环节,请根据下列实验要求回答相关问题。
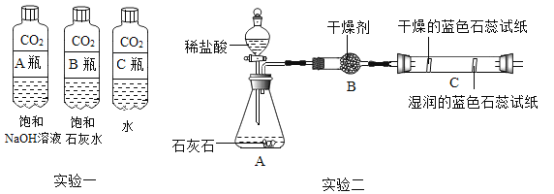
(1)实验一中振荡三个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生反应的化学方程式为_____;对比A瓶与_____(填“B”或“C”)瓶的实验现象,可证明二氧化碳能与氢氧化钠发生反应。
(2)实验二观察到C装置中发生的现象是干燥的蓝色石蕊试纸不变色,而湿润的蓝色石蕊试纸变_____色,结论是_____.(用化学方程式表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】李克强总理在十三届全国人大一次会议报告中,要求通过技术创新、产业转型、新能源开发等多种手段,尽可能地减少高碳能源消耗,达到经济社会发展与生态环境保护双赢的一种经济发展形态。
(1)氢气被视为21世纪最有发展的新型“绿色能源”原因是:因其制取原料来源广,燃烧放热大,_____等特点。
(2)天然气是一种重要的“非石油化”能源,请回答下列问题:
①甲烷与氧气构成的燃料电池中能量转化形式主要是_____。
a.化学能转化为热能 b.电能转化为化学能 c.化学能转化为电能
②将CH4和CO2在一定条件下生成CO和H2时,该反应的重大意义是_____。
(3)可燃冰是在高压低温环境条件下,水分子笼中装有甲烷分子而成的“冰块”,可直接点燃。甲烷在空气中充分燃烧的化学方程式是_____。
(4)开采可燃冰矿藏的关键技术之一是防止其泄漏,如果开采过程中大量气体泄漏,会比二氧化碳造成的_____更严重。
(5)石油可以炼制液化石油气,液化石油气的主要成分是丙烷(C3H8)、丁烷(C4H10)等。丁烷燃烧的化学方程式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com