
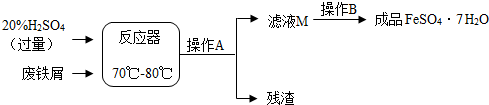
·ĻĢśŠ¼µÄÖ÷ŅŖ³É·ŻŹĒĢś£¬Ķ¬Ź±»¹ÓŠÉŁĮæĢśŠā£ØFe2O3£©£¬¶ÆĪļĖĒĮĻĮņĖįŃĒĢśµÄÉś²ś¹¤ŅÕÖ®Ņ»ČēĻĀĶ¼ĖłŹ¾£ŗ

£Ø1£©ŌŚ·“Ó¦Ę÷ÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½³żFe2(SO4)3+Fe=3FeSO4Ķā»¹ÓŠ£ŗ £»
£Ø2£©ĀĖŅŗMÖŠæĻ¶Øŗ¬ÓŠµÄČÜÖŹµÄ»ÆѧŹ½ŹĒ £»
£Ø3£©ŌŚŹµŃéŹŅÖŠĶź³É²Ł×÷AµÄ²£Į§ŅĒĘ÷ÓŠ²£Į§°ō”¢ÉÕ±ŗĶ £»
£Ø4£©ĀĖŅŗM¾¹ż²Ł×÷BæɵĆĮņĖįŃĒĢś¾§Ģå(FeSO4”¤7H2O)”£ŅŃÖŖĮņĖįŃĒĢśµÄČܽā¶ČŗĶĪö³ö¾§ĢåµÄ×é³ÉČēĻĀ±ķ£ŗ
|
ĪĀ¶Č/”ę |
0 |
10 |
30 |
40 |
50 |
60 |
64 |
70 |
80 |
90 |
|
|
Čܽā¶Č/g |
15.6 |
20.5 |
33.0 |
40.4 |
48.8 |
55.0 |
55.3 |
50.6 |
43.7 |
37.2 |
|
|
Īö³ö¾§Ģå |
FeSO4”¤7H2O |
FeSO4”¤4H2O |
FeSO4”¤H2O |
||||||||
øł¾ŻČܽā¶Č±ķ£¬ĮņĖįŃĒĢś¾§Ģå(FeSO4”¤7H2O)ĄäČ“½į¾§ĪĀ¶Č×īøß²»³¬¹ż ”ę£»
£Ø5£©ŌŚ»Æѧ·“Ó¦ÖŠ£¬ČōÓŠŌŖĖŲ»ÆŗĻ¼Ū±ä»ÆµÄ·“Ó¦¶ØŅåĪŖŃõ»Æ»¹Ō·“Ó¦”£ĻĀĮŠ·“Ó¦ĄąŠĶæĻ¶ØŹĒŃõ»Æ»¹Ō·“Ó¦µÄŹĒ £ØĢī×ÖÄø±ąŗÅ£©£»
A.»ÆŗĻ·“Ó¦ B.ÖĆ»»·“Ó¦ C.·Ö½ā·“Ó¦ D.ø“·Ö½ā·“Ó¦
ŌŚŃõ»Æ»¹Ō·“Ó¦ÖŠ£¬ČōÓŠŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ¬±ŲÓŠŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬ĒŅŌŖĖŲ»ÆŗĻ¼ŪÉż½µ×ÜŹżĻąµČ”£
½«ĪŽĖ®ĮņĖįŃĒĢś£ØFeSO4£©øō¾ųæÕĘų¼ÓĒæČČ£¬Éś³É²śĪļÓŠČżŃõ»Æ¶žĢśŗĶĘäĖüŃõ»ÆĪļ£¬ŹŌŠ“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ ”£
£Ø1£©Fe+H2SO4= FeSO4+ H2”ü£Ø2·Ö£©; Fe2O3+3 H2SO4= Fe2(SO4)3+3 H2O£Ø2·Ö£©
£Ø2£©FeSO4”¢H2SO4£Ø2·Ö£¬Ćæ¶Ō1øöøų1·Ö£©
£Ø3£©Ā©¶· £Ø2·Ö£© £Ø4£©64 £Ø1·Ö£©
£Ø5£©B £Ø1·Ö£©£»2FeSO4  Fe2O3+
SO2+ SO3£Ø2·Ö£¬»ņĒæČČ£¬ĘųĢå·ūŗÅæɲ»æŪ·Ö£©
Fe2O3+
SO2+ SO3£Ø2·Ö£¬»ņĒæČČ£¬ĘųĢå·ūŗÅæɲ»æŪ·Ö£©
”¾½āĪö”æ£Ø1£©·“Ó¦Ę÷ÖŠµÄĪļÖŹÓŠFe ”¢Fe2O3”¢H2SO4 ”£H2SO4»¹æÉÓėFe·“Ó¦£ØĖįÓė½šŹō·“Ó¦£©”¢ÓėFe2O3·“Ó¦£ØĖįÓė½šŹōŃõ»ÆĪļ·“Ó¦£©”£ĖłŅŌ»¹“ęŌŚµÄ·“Ó¦ĪŖ£ŗ Fe+H2SO4= FeSO4+ H2”ü Fe2O3+3 H2SO4= Fe2(SO4)3+3 H2O
£Ø2£©ĀĖŅŗ¾¹ż²Ł×÷BæɵĆFeSO4”¤7H2O£¬ĖłŅŌŅ»¶Øŗ¬FeSO4£¬Ņņ²ĪÓė·“Ó¦µÄH2SO4ŹĒ¹żĮæµÄ£¬ĖłŅŌ»¹Ņ»¶Øŗ¬ÓŠH2SO4”£
£Ø3£©²Ł×÷AµÄ×÷ÓĆŹĒ½«·“Ó¦Ę÷ÖŠµÄĪļÖŹ·Ö³ÉĮĖ¹ĢĢ岊ŌüŗĶŅŗĢåĀĖŅŗM£¬¼“·ÖĄė¹ĢĢåŗĶŅŗĢ壬Ņņ“Ė²Ł×÷AÓ¦ĪŖ¹żĀĖ”£¹żĀĖ»¹ŅŖÓƵ½µÄ²£Į§ŅĒĘ÷ŹĒĀ©¶·”£
£Ø4£©øł¾ŻČܽā¶Č±ķæÉÖŖĮņĖįŃĒĢś¾§Ģå(FeSO4”¤7H2O)Īö³ö½į¾§µÄĪĀ¶Č·¶Ī§ŹĒ0”ęÖĮ64”ę£¬ĖłŅŌĄäČ“½į¾§ĪĀ¶Č×īøß²»Äܳ¬¹ż64”ę”£
£Ø5£©A.»ÆŗĻ·“Ó¦ÖŠŌŖĖŲµÄ»ÆŗĻ¼ŪæÉÄÜ·¢Éś±ä»Æ”£Čē£ŗCaO+H2O”śCa£ØOH£©2ÖŠŌŖĖŲµÄ»ÆŗĻ¼Ūƻӊ·¢Éś±ä»Æ£»H2+O2 H2OÖŠHŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ0¼ŪÉżøßĪŖ+1¼Ū”¢OŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ0¼ŪÄæ½µµĶĪŖ”Ŗ2¼Ū”£
H2OÖŠHŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ0¼ŪÉżøßĪŖ+1¼Ū”¢OŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ0¼ŪÄæ½µµĶĪŖ”Ŗ2¼Ū”£
B.ÖĆ»»·“Ó¦ÖŠŅ»¶ØÓŠŌŖĖŲµÄ»ÆŗĻ¼Ū·¢Éś±ä»Æ”£Čē£ŗ Fe+H2SO4= FeSO4+ H2”üÖŠFeŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ0¼ŪÉżøßĪŖ+2¼Ū£¬HŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ+1¼Ū½µĪŖ0¼Ū”£
C.·Ö½ā·“Ó¦ÖŠŌŖĖŲµÄ»ÆŗĻ¼ŪæÉÄÜ·¢Éś±ä»Æ”£Čē£ŗH2CO3=H2O+CO2”üÖŠŌŖĖŲµÄ»ÆŗĻ¼ŪĪ“·¢Éś±ä»Æ£»H2O H2”ü+O2”üÖŠHŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ+1¼Ū½µĪŖ0¼Ū£¬OŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ”Ŗ2¼ŪÉżøßĪŖ0¼Ū”£
H2”ü+O2”üÖŠHŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ+1¼Ū½µĪŖ0¼Ū£¬OŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ”Ŗ2¼ŪÉżøßĪŖ0¼Ū”£
D.ø“·Ö½ā·“Ó¦ÖŠŌŖĖŲµÄ»ÆŗĻ¼Ū²»·¢Éś±ä»Æ”£Čē£ŗNaOH+HCl=NaCl+H2OÖŠø÷ŌŖĖŲµÄ»ÆŗĻ¼Ūƻӊ·¢Éś±ä»Æ”£
ĖłŅŌŅ»¶ØæĻ¶ØŹĒŃõ»Æ»¹Ō·“Ó¦µÄŹĒÖĆ»»·“Ó¦”£
øł¾ŻÖŹĮæŹŲŗć¶ØĀÉæÉÖŖÉś³ÉµÄĘäĖüŃõ»ÆĪļÖŠæĻ¶ØÓŠĮņŌŖĖŲ”£ĮņµÄŃõ»ÆĪļÓŠ¶žŃõ»ÆĮņÓėČżŃõ»ÆĮņ”£øł¾ŻFeSO4”¢SO2”¢SO3ÖŠŌ×ÓøöŹż±Č¼ĘĖćæÉÖŖÉś³ÉĪļÖŠÓ¦ŗ¬ÓŠSO2”¢SO3”£Ōņ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2FeSO4
 Fe2O3+
SO2ӟ+ SO3ӟ
Fe2O3+
SO2ӟ+ SO3ӟ
æ¼µć£ŗĪļÖŹ¼äµÄ·“Ó¦”¢ÖŹĮæŹŲŗć¶ØĀÉ”¢¹żĀĖ”¢»Æѧ·½³ĢŹ½µÄŹéŠ“
µćĘĄ£ŗ±¾Ģā¶ŌѧɜµÄ·ÖĪöÄÜĮ¦ŅŖĒó½Ļøß”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ĪĀ¶Č/”ę | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 | |
| Čܽā¶Č/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 | |
| Īö³ö¾§Ģå | FeSO4?7H2O | FeSO4?4H2O | FeSO4?H2O | ||||||||
| ||
| ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ2013Äź³õÖŠ±ĻŅµÉżŃ§æ¼ŹŌ£ØĖÄ“ØŃÅ°²¾ķ£©»Æѧ£Ø“ų½āĪö£© ĢāŠĶ£ŗĪŹ“šĢā
·ĻĢśŠ¼µÄÖ÷ŅŖ³É·ŻŹĒĢś£¬Ķ¬Ź±»¹ÓŠÉŁĮæĢśŠā£ØFe2O3£©£¬¶ÆĪļĖĒĮĻĮņĖįŃĒĢśµÄÉś²ś¹¤ŅÕÖ®Ņ»ČēĻĀĶ¼ĖłŹ¾£ŗ
£Ø1£©ŌŚ·“Ó¦Ę÷ÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½³żFe2(SO4)3+Fe=3FeSO4Ķā»¹ÓŠ£ŗ £»
£Ø2£©ĀĖŅŗMÖŠæĻ¶Øŗ¬ÓŠµÄČÜÖŹµÄ»ÆѧŹ½ŹĒ £»
£Ø3£©ŌŚŹµŃéŹŅÖŠĶź³É²Ł×÷AµÄ²£Į§ŅĒĘ÷ÓŠ²£Į§°ō”¢ÉÕ±ŗĶ £»
£Ø4£©ĀĖŅŗM¾¹ż²Ł×÷BæɵĆĮņĖįŃĒĢś¾§Ģå(FeSO4”¤7H2O)”£ŅŃÖŖĮņĖįŃĒĢśµÄČܽā¶ČŗĶĪö³ö¾§ĢåµÄ×é³ÉČēĻĀ±ķ£ŗ
| ĪĀ¶Č/”ę | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 | |
| Čܽā¶Č/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 | |
| Īö³ö¾§Ģå | FeSO4”¤7H2O | FeSO4”¤4H2O | FeSO4”¤H2O | ||||||||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

| ĪĀ¶Č/”ę | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 | |
| Čܽā¶Č/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 | |
| Īö³ö¾§Ģå | FeSO4?7H2O | FeSO4?4H2O | FeSO4?H2O | ||||||||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ2013ÄźĖÄ“ØŹ”ŃÅ°²ŹŠÖŠæ¼»ÆѧŹ½¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā

| ĪĀ¶Č/”ę | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 | ||
| Čܽā¶Č/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 | |
| Īö³ö¾§Ģå | FeSO4?7H2O | FeSO4?4H2O | FeSO4?H2O | ||||||||
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com