
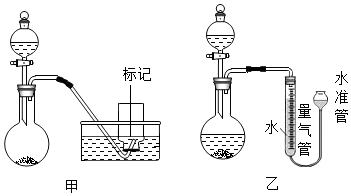
分析 (1)根据气体的密度容易受温度和压强的影响进行分析;
(2)根据题中共收集了10瓶氧气,因此总体积是10V0,依据密度公式:ρ=$\frac{m}{V}$进行分析;
(3)根据保持量气装置使两边液面相平时,保持水准管静止,待水准管中液面不再上升时再读数,内外压强就相等,才不会出现误差进行分析;
(4)根据如果实验中装置气密性不好,测得的氧气的密度会偏大,收集一定体积氧气时,由于部分氧气泄漏导致消耗的过氧化氢质量增加,使测得氧气的质量偏大进行分析.
解答 解:(1)气体的密度容易受温度和压强的影响,所以步骤四中,控制集气瓶内、外液面保持相平的目的是:使集气瓶中的气压和烧瓶中的气压相等;
(2)题中共收集了10瓶氧气,因此总体积是10V0,由密度公式可知:ρ=$\frac{m}{V}$=$\frac{{m}_{1}-{m}_{2}}{10{V}_{0}}$克/毫升,与真实值比较将偏大,理由是:氧气中带有水蒸气,装置内减少质量变大;
(3)保持量气装置使两边液面相平时,保持水准管静止,待水准管中液面不再上升时再读数,内外压强就相等,才不会出现误差,故选:AB;
(4)如果实验中装置气密性不好,测得的氧气的密度会偏大,收集一定体积氧气时,由于部分氧气泄漏导致消耗的过氧化氢质量增加,使测得氧气的质量偏大.
故答案为:(1)使集气瓶中的气压和烧瓶中的气压相等;
(2)$\frac{{m}_{1}-{m}_{2}}{10{V}_{0}}$,偏大,氧气中带有水蒸气,装置内减少质量变大;
(3)AB;
(4)偏大,收集一定体积氧气时,由于部分氧气泄漏导致消耗的过氧化氢质量增加,使测得氧气的质量偏大.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 糖水 | B. | 食醋 | C. | 酱油 | D. | 清水 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碱-①④ | B. | 纯净物-①③④⑤ | C. | 氧化物-⑤⑥ | D. | 盐-①⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 浓硫酸、浓盐酸 | B. | 浓盐酸、氢氧化钠溶液 | ||
| C. | 氢氧化钠溶液、食盐水 | D. | 浓硫酸、氢氧化钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com