

| ||
| ||


科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
| 过氧化氢溶液浓度∕% | 过氧化氢溶液体积∕m L | 温度∕℃ | 二氧化锰的用量∕g | 收集氧气的体积∕m L | 反应所需的时间∕s | |
| Ⅰ | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| Ⅱ | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| Ⅲ | 30 | 5 | 35 | 2 | 49.21 | |
| Ⅳ | 30 | 5 | 55 | 2 | 10.76 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
 2008年初,我国南方地区遭受了一场特大雪灾,道路结冰,给交通带来极大不便.为了快速消除道路上的积雪,交通部门使用了大量的融雪剂,某公司生产的融雪剂是由NaCl、CaCl2、Na2CO3和CuSO4中的一种或两种物质组成.化学兴趣小组的小红和小兰对融雪剂产生很大的兴趣并对融雪剂的成分进行积极的探究.
2008年初,我国南方地区遭受了一场特大雪灾,道路结冰,给交通带来极大不便.为了快速消除道路上的积雪,交通部门使用了大量的融雪剂,某公司生产的融雪剂是由NaCl、CaCl2、Na2CO3和CuSO4中的一种或两种物质组成.化学兴趣小组的小红和小兰对融雪剂产生很大的兴趣并对融雪剂的成分进行积极的探究.| 步骤 | 操作 | 现象 |
| Ⅰ | 加水溶解 | 得无色澄清溶液 |
| Ⅱ | 加入Na2CO3溶液 | 生成白色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:
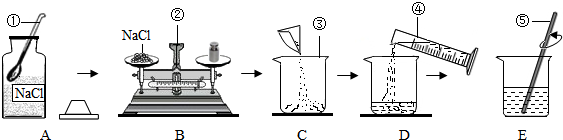
查看答案和解析>>
科目:初中化学 来源: 题型:
 去年冬天至今年春天,我国西南地区遭遇大范围持续干旱.全国人民团结一致,共同抗旱.
去年冬天至今年春天,我国西南地区遭遇大范围持续干旱.全国人民团结一致,共同抗旱.查看答案和解析>>
科目:初中化学 来源: 题型:
 某学生拟通过测定粗锌(杂质与稀硫酸不反应)与稀硫酸反应产生的气体体积,来测定粗锌中锌的纯度.现有粗锌、稀硫酸、试管、镊子、单孔橡皮塞、导气管、托盘天平、量筒、水槽、铁架台(附铁夹)等仪器、药品.
某学生拟通过测定粗锌(杂质与稀硫酸不反应)与稀硫酸反应产生的气体体积,来测定粗锌中锌的纯度.现有粗锌、稀硫酸、试管、镊子、单孔橡皮塞、导气管、托盘天平、量筒、水槽、铁架台(附铁夹)等仪器、药品.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com