
Ķ¬Ń§ĆĒ¶¼ÖŖµĄCuSO4ČÜŅŗ³ŹĄ¶É«£¬ÄĒĆ“£¬ÄćĆĒÖŖµĄŹĒČÜŅŗÖŠŹ²Ć“Ī¢Į£Ź¹CuSO4ČÜŅŗ³ŹĄ¶É«Āš£æ
»łÓŚ³õÖŠĖłŃ§ÖŖŹ¶£¬ĻĀĆęÖ÷ŅŖ²ÉÓĆ²»Ķ¬µÄĖ¼Ī¬·½Ź½¶ŌøĆĪŹĢā½ųŠŠĢ½ĢÖ£®
£ØĖµĆ÷£ŗŅŌĻĀČÜŅŗ½ŌĪŖĻ”ČÜŅŗ£¬ŌŚĻ”ČÜŅŗÖŠSO42﹣”¢Cl﹣³ŹĪŽÉ«£®£©
Ė¼Ā·Ņ»£ŗ²ÉÓĆ¹éÄÉ·Ø£¬ÓɾßĢåŹĀŹµĶĘĄķøÅĄØ³öŅ»°ćŌĄķ»ņ½įĀŪ£®
ĻĀĶ¼Ņ»£ŗĒė±Č½ĻA”¢B”¢C”¢D”¢EĪåÖ§ŹŌ¹ÜÖŠĖłŹ¢ŹŌ¼ĮµÄŃÕÉ«ÓėĖłŗ¬Ī¢Į££¬½ųŠŠ·ÖĪö£®
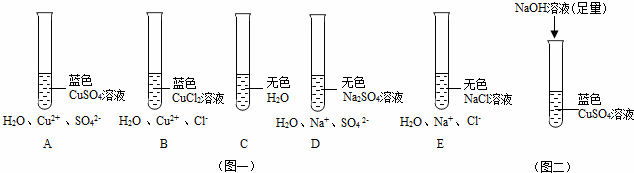
¶Ō A”¢B”¢CµÄ·ÖĪöŹĒ£ŗ””””£¬ĖµĆ÷Cu2+µÄ“ęŌŚŹ¹CuSO4”¢CuCl2ČÜŅŗĻŌĄ¶É«£®
¶Ō””””·ÖĪö£¬æÉŅŌĖµĆ÷£¬ŌŚĖ®ČÜŅŗÖŠ£¬Na+ŹĒĪŽÉ«µÄ£®
¶ŌA”¢DµÄ·ÖĪöŹĒ£ŗ””””£¬ĖµĆ÷AÖŠŹĒCu2+Ź¹CuSO4ČÜŅŗĻŌĄ¶É«£®¶ŌB”¢E·ÖĪöĶ¬Ąķ£®
¶ŌA”¢B”¢C”¢D”¢E »¹æÉĶĘĄķ£ŗĖ®ŹĒĪŽÉ«ŅŗĢ壬×÷ĪŖČܼĮ£¬ČܽāCuSO4”¢CuCl2µČĪļÖŹŹ±£¬ČÜŅŗµÄŃÕÉ«Ö÷ŅŖŹÜČÜÖŹµÄÓ°Ļģ£®
Ė¼Ā·¶ž£ŗ²ÉÓĆ¼ÓČėŹŌ¼Į·¢Éś»Æѧ·“Ó¦µÄ·½·Ø½«ČÜŅŗÖŠµÄCu2+³żČ„»ņ±£³ÖČÜŅŗÖŠCu2+µÄ“ęŌŚ£¬¹Ū²ģČÜŅŗŃÕÉ«ŹĒ·ń±ä»ÆµÄ·½·Ø£®
Ąż1£ŗČēĶ¼¶žĖłŹ¾µÄ·½·ØŹĒ³żČ„ČÜŅŗÖŠµÄCu2+£®øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ””””£®
Ąż2£ŗĒėŃ”ŌńŅ»ÖÖŹŌ¼ĮÓėCuSO4ČÜŅŗ·“Ó¦£¬±£³ÖČÜŅŗÖŠCu2+ µÄ“ęŌŚ£®Ęä»Æѧ·½³ĢŹ½ŹĒ£ŗ””””£®
ÉĻŹöŃŠ¾æ·½·ØŹĒÓĆ²»Ķ¬µÄĖ¼Ī¬·½Ź½£¬“Ó²»Ķ¬µÄĒŠČėµćŃŠ¾æĶ¬Ņ»øöĪŹĢā£¬µ«×ÜĢåĖ¼Ā·ČŌČ»ŹĒ¶Ō±ČŹµŃéÉč¼ĘµÄŅ»°ćĖ¼Ā·£®
| ½ā£ŗøł¾ŻA”¢B”¢CČżÖ§ŹŌ¹ÜÖŠĖłŹ¢ŹŌ¼ĮµÄŃÕÉ«ÓėĖłŗ¬Ī¢Į££¬Ė®ŹĒĪŽÉ«µÄ£¬A”¢BµÄČÜŅŗÖŠ¾łŗ¬Cu2+£¬¾łĻŌĄ¶É«£¬ĖµĆ÷Cu2+µÄ“ęŌŚŹ¹CuSO4”¢CuCl2ČÜŅŗĻŌĄ¶É«£® D”¢EĮ½Ö§ŹŌ¹ÜÖŠ¾łŗ¬ÄĘĄė×Ó£¬øł¾ŻĢāŅā£¬ŌŚĻ”ČÜŅŗÖŠSO42﹣”¢Cl﹣³ŹĪŽÉ«£¬ĖµĆ÷ŌŚĖ®ČÜŅŗÖŠ£¬Na+ŹĒĪŽÉ«µÄ£® øł¾Ż¶ŌA”¢DµÄ·ÖĪö£¬A”¢DµÄČÜŅŗÖŠ¾łŗ¬Ė®·Ö×Ó”¢ĮņĖįøłĄė×Ó£¬Ė®·Ö×Ó²»ÄÜŹ¹ČÜŅŗĻŌĄ¶É«£¬ŌŚĻ”ČÜŅŗÖŠSO42﹣³ŹĪŽÉ«£¬ĖµĆ÷AÖŠŹĒCu2+Ź¹CuSO4ČÜŅŗĻŌĄ¶É«£® ČēĶ¼¶žĖłŹ¾µÄ·½·ØŹĒ³żČ„ČÜŅŗÖŠµÄCu2+£¬ŹĒĒāŃõ»ÆÄĘÓėĮņĖįĶ·“Ӧɜ³ÉĒāŃõ»ÆĶ³ĮµķŗĶĮņĖįÄĘ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2NaOH+CuSO4=Cu£ØOH£©2”ż+Na2SO4£» Ń”ŌńŅ»ÖÖŹŌ¼ĮÓėCuSO4ČÜŅŗ·“Ó¦£¬±£³ÖČÜŅŗÖŠCu2+ µÄ“ęŌŚ£¬æÉŃ”ÓĆĀČ»Æ±µÓėĮņĖįĶ·“Ó¦£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCuSO4+BaCl2=BaSO4”ż+CuCl2£® ¹Ź“š°øĪŖ£ŗA”¢BČÜŅŗÖŠ¾łŗ¬Cu2+£¬¾łĻŌĄ¶É«£»D”¢E£»A”¢DµÄČÜŅŗÖŠ¾łŗ¬Ė®·Ö×Ó”¢ĮņĖįøłĄė×Ó£¬Ė®·Ö×Ó²»ÄÜŹ¹ČÜŅŗĻŌĄ¶É«£¬ŌŚĻ”ČÜŅŗÖŠSO42﹣³ŹĪŽÉ«£» 2NaOH+CuSO4=Cu£ØOH£©2”ż+Na2SO4£»CuSO4+BaCl2=BaSO4”ż+CuCl2£» |
””ѧæĘĶõ


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ2012Äź³õÖŠ±ĻŅµÉżŃ§æ¼ŹŌ£Øŗž±±ĢģĆžķ£©»Æѧ£Ø“ų½āĪö£© ĢāŠĶ£ŗĢ½¾æĢā
£Ø5·Ö£©£Ø2012?ĻÉĢŅ£©Ķ¬Ń§ĆĒ¶¼ÖŖµĄCuSO4ČÜŅŗ³ŹĄ¶É«£¬ÄĒĆ“£¬ÄćĆĒÖŖµĄŹĒČÜŅŗÖŠŹ²Ć“Ī¢Į£Ź¹CuSO4ČÜŅŗ³ŹĄ¶É«Āš£æ
»łÓŚ³õÖŠĖłŃ§ÖŖŹ¶£¬ĻĀĆęÖ÷ŅŖ²ÉÓĆ²»Ķ¬µÄĖ¼Ī¬·½Ź½¶ŌøĆĪŹĢā½ųŠŠĢ½ĢÖ£®
£ØĖµĆ÷£ŗŅŌĻĀČÜŅŗ½ŌĪŖĻ”ČÜŅŗ£¬ŌŚĻ”ČÜŅŗÖŠSO42©”¢Cl©³ŹĪŽÉ«£®£©
Ė¼Ā·Ņ»£ŗ²ÉÓĆ¹éÄÉ·Ø£¬ÓɾßĢåŹĀŹµĶĘĄķøÅĄØ³öŅ»°ćŌĄķ»ņ½įĀŪ£®
ĻĀĶ¼Ņ»£ŗĒė±Č½ĻA”¢B”¢C”¢D”¢EĪåÖ§ŹŌ¹ÜÖŠĖłŹ¢ŹŌ¼ĮµÄŃÕÉ«ÓėĖłŗ¬Ī¢Į££¬½ųŠŠ·ÖĪö£®
¶Ō A”¢B”¢CµÄ·ÖĪöŹĒ£ŗ””_________””£¬ĖµĆ÷Cu2+µÄ“ęŌŚŹ¹CuSO4”¢CuCl2ČÜŅŗĻŌĄ¶É«£®
¶Ō””_________””·ÖĪö£¬æÉŅŌĖµĆ÷£¬ŌŚĖ®ČÜŅŗÖŠ£¬Na+ŹĒĪŽÉ«µÄ£®
¶ŌA”¢DµÄ·ÖĪöŹĒ£ŗ””_________””£¬ĖµĆ÷AÖŠŹĒCu2+Ź¹CuSO4ČÜŅŗĻŌĄ¶É«£®¶ŌB”¢E·ÖĪöĶ¬Ąķ£®
¶ŌA”¢B”¢C”¢D”¢E »¹æÉĶĘĄķ£ŗĖ®ŹĒĪŽÉ«ŅŗĢ壬×÷ĪŖČܼĮ£¬ČܽāCuSO4”¢CuCl2µČĪļÖŹŹ±£¬ČÜŅŗµÄŃÕÉ«Ö÷ŅŖŹÜČÜÖŹµÄÓ°Ļģ£®
Ė¼Ā·¶ž£ŗ²ÉÓĆ¼ÓČėŹŌ¼Į·¢Éś»Æѧ·“Ó¦µÄ·½·Ø½«ČÜŅŗÖŠµÄCu2+³żČ„»ņ±£³ÖČÜŅŗÖŠCu2+µÄ“ęŌŚ£¬¹Ū²ģČÜŅŗŃÕÉ«ŹĒ·ń±ä»ÆµÄ·½·Ø£®
Ąż1£ŗČēĶ¼¶žĖłŹ¾µÄ·½·ØŹĒ³żČ„ČÜŅŗÖŠµÄCu2+£®øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ””_________””£®
Ąż2£ŗĒėŃ”ŌńŅ»ÖÖŹŌ¼ĮÓėCuSO4ČÜŅŗ·“Ó¦£¬±£³ÖČÜŅŗÖŠCu2+µÄ“ęŌŚ£®Ęä»Æѧ·½³ĢŹ½ŹĒ£ŗ””_________””£®
ÉĻŹöŃŠ¾æ·½·ØŹĒÓĆ²»Ķ¬µÄĖ¼Ī¬·½Ź½£¬“Ó²»Ķ¬µÄĒŠČėµćŃŠ¾æĶ¬Ņ»øöĪŹĢā£¬µ«×ÜĢåĖ¼Ā·ČŌČ»ŹĒ¶Ō±ČŹµŃéÉč¼ĘµÄŅ»°ćĖ¼Ā·£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ2012Äź³õÖŠ±ĻŅµÉżŃ§æ¼ŹŌ£Øŗž±±ĻÉĢŅ¾ķ£©»Æѧ£Ø“ų½āĪö£© ĢāŠĶ£ŗĢ½¾æĢā
£Ø5·Ö£©£Ø2012?ĻÉĢŅ£©Ķ¬Ń§ĆĒ¶¼ÖŖµĄCuSO4ČÜŅŗ³ŹĄ¶É«£¬ÄĒĆ“£¬ÄćĆĒÖŖµĄŹĒČÜŅŗÖŠŹ²Ć“Ī¢Į£Ź¹CuSO4ČÜŅŗ³ŹĄ¶É«Āš£æ
»łÓŚ³õÖŠĖłŃ§ÖŖŹ¶£¬ĻĀĆęÖ÷ŅŖ²ÉÓĆ²»Ķ¬µÄĖ¼Ī¬·½Ź½¶ŌøĆĪŹĢā½ųŠŠĢ½ĢÖ£®
£ØĖµĆ÷£ŗŅŌĻĀČÜŅŗ½ŌĪŖĻ”ČÜŅŗ£¬ŌŚĻ”ČÜŅŗÖŠSO42©”¢Cl©³ŹĪŽÉ«£®£©
Ė¼Ā·Ņ»£ŗ²ÉÓĆ¹éÄÉ·Ø£¬ÓɾßĢåŹĀŹµĶĘĄķøÅĄØ³öŅ»°ćŌĄķ»ņ½įĀŪ£®
ĻĀĶ¼Ņ»£ŗĒė±Č½ĻA”¢B”¢C”¢D”¢EĪåÖ§ŹŌ¹ÜÖŠĖłŹ¢ŹŌ¼ĮµÄŃÕÉ«ÓėĖłŗ¬Ī¢Į££¬½ųŠŠ·ÖĪö£®
¶Ō A”¢B”¢CµÄ·ÖĪöŹĒ£ŗ”” ””£¬ĖµĆ÷Cu2+µÄ“ęŌŚŹ¹CuSO4”¢CuCl2ČÜŅŗĻŌĄ¶É«£®
¶Ō”” ””·ÖĪö£¬æÉŅŌĖµĆ÷£¬ŌŚĖ®ČÜŅŗÖŠ£¬Na+ŹĒĪŽÉ«µÄ£®
¶ŌA”¢DµÄ·ÖĪöŹĒ£ŗ”” ””£¬ĖµĆ÷AÖŠŹĒCu2+Ź¹CuSO4ČÜŅŗĻŌĄ¶É«£®¶ŌB”¢E·ÖĪöĶ¬Ąķ£®
¶ŌA”¢B”¢C”¢D”¢E »¹æÉĶĘĄķ£ŗĖ®ŹĒĪŽÉ«ŅŗĢ壬×÷ĪŖČܼĮ£¬ČܽāCuSO4”¢CuCl2µČĪļÖŹŹ±£¬ČÜŅŗµÄŃÕÉ«Ö÷ŅŖŹÜČÜÖŹµÄÓ°Ļģ£®
Ė¼Ā·¶ž£ŗ²ÉÓĆ¼ÓČėŹŌ¼Į·¢Éś»Æѧ·“Ó¦µÄ·½·Ø½«ČÜŅŗÖŠµÄCu2+³żČ„»ņ±£³ÖČÜŅŗÖŠCu2+µÄ“ęŌŚ£¬¹Ū²ģČÜŅŗŃÕÉ«ŹĒ·ń±ä»ÆµÄ·½·Ø£®
Ąż1£ŗČēĶ¼¶žĖłŹ¾µÄ·½·ØŹĒ³żČ„ČÜŅŗÖŠµÄCu2+£®øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ”” ””£®
Ąż2£ŗĒėŃ”ŌńŅ»ÖÖŹŌ¼ĮÓėCuSO4ČÜŅŗ·“Ó¦£¬±£³ÖČÜŅŗÖŠCu2+µÄ“ęŌŚ£®Ęä»Æѧ·½³ĢŹ½ŹĒ£ŗ”” ””£®
ÉĻŹöŃŠ¾æ·½·ØŹĒÓĆ²»Ķ¬µÄĖ¼Ī¬·½Ź½£¬“Ó²»Ķ¬µÄĒŠČėµćŃŠ¾æĶ¬Ņ»øöĪŹĢā£¬µ«×ÜĢåĖ¼Ā·ČŌČ»ŹĒ¶Ō±ČŹµŃéÉč¼ĘµÄŅ»°ćĖ¼Ā·£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ2012Äź³õÖŠ±ĻŅµÉżŃ§æ¼ŹŌ£Øŗž±±ĢģĆžķ£©»Æѧ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢ½¾æĢā
£Ø5·Ö£©£Ø2012•ĻÉĢŅ£©Ķ¬Ń§ĆĒ¶¼ÖŖµĄCuSO4ČÜŅŗ³ŹĄ¶É«£¬ÄĒĆ“£¬ÄćĆĒÖŖµĄŹĒČÜŅŗÖŠŹ²Ć“Ī¢Į£Ź¹CuSO4ČÜŅŗ³ŹĄ¶É«Āš£æ
»łÓŚ³õÖŠĖłŃ§ÖŖŹ¶£¬ĻĀĆęÖ÷ŅŖ²ÉÓĆ²»Ķ¬µÄĖ¼Ī¬·½Ź½¶ŌøĆĪŹĢā½ųŠŠĢ½ĢÖ£®
£ØĖµĆ÷£ŗŅŌĻĀČÜŅŗ½ŌĪŖĻ”ČÜŅŗ£¬ŌŚĻ”ČÜŅŗÖŠSO42©”¢Cl©³ŹĪŽÉ«£®£©
Ė¼Ā·Ņ»£ŗ²ÉÓĆ¹éÄÉ·Ø£¬ÓɾßĢåŹĀŹµĶĘĄķøÅĄØ³öŅ»°ćŌĄķ»ņ½įĀŪ£®
ĻĀĶ¼Ņ»£ŗĒė±Č½ĻA”¢B”¢C”¢D”¢EĪåÖ§ŹŌ¹ÜÖŠĖłŹ¢ŹŌ¼ĮµÄŃÕÉ«ÓėĖłŗ¬Ī¢Į££¬½ųŠŠ·ÖĪö£®
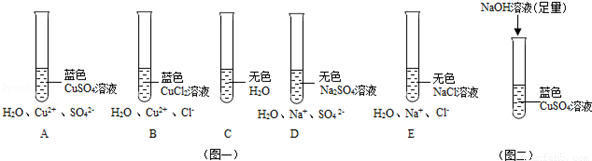
¶Ō A”¢B”¢CµÄ·ÖĪöŹĒ£ŗ””_________””£¬ĖµĆ÷Cu2+µÄ“ęŌŚŹ¹CuSO4”¢CuCl2ČÜŅŗĻŌĄ¶É«£®
¶Ō””_________””·ÖĪö£¬æÉŅŌĖµĆ÷£¬ŌŚĖ®ČÜŅŗÖŠ£¬Na+ŹĒĪŽÉ«µÄ£®
¶ŌA”¢DµÄ·ÖĪöŹĒ£ŗ””_________””£¬ĖµĆ÷AÖŠŹĒCu2+Ź¹CuSO4ČÜŅŗĻŌĄ¶É«£®¶ŌB”¢E·ÖĪöĶ¬Ąķ£®
¶ŌA”¢B”¢C”¢D”¢E »¹æÉĶĘĄķ£ŗĖ®ŹĒĪŽÉ«ŅŗĢ壬×÷ĪŖČܼĮ£¬ČܽāCuSO4”¢CuCl2µČĪļÖŹŹ±£¬ČÜŅŗµÄŃÕÉ«Ö÷ŅŖŹÜČÜÖŹµÄÓ°Ļģ£®
Ė¼Ā·¶ž£ŗ²ÉÓĆ¼ÓČėŹŌ¼Į·¢Éś»Æѧ·“Ó¦µÄ·½·Ø½«ČÜŅŗÖŠµÄCu2+³żČ„»ņ±£³ÖČÜŅŗÖŠCu2+µÄ“ęŌŚ£¬¹Ū²ģČÜŅŗŃÕÉ«ŹĒ·ń±ä»ÆµÄ·½·Ø£®
Ąż1£ŗČēĶ¼¶žĖłŹ¾µÄ·½·ØŹĒ³żČ„ČÜŅŗÖŠµÄCu2+£®øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ””_________””£®
Ąż2£ŗĒėŃ”ŌńŅ»ÖÖŹŌ¼ĮÓėCuSO4ČÜŅŗ·“Ó¦£¬±£³ÖČÜŅŗÖŠCu2+ µÄ“ęŌŚ£®Ęä»Æѧ·½³ĢŹ½ŹĒ£ŗ””_________””£®
ÉĻŹöŃŠ¾æ·½·ØŹĒÓĆ²»Ķ¬µÄĖ¼Ī¬·½Ź½£¬“Ó²»Ķ¬µÄĒŠČėµćŃŠ¾æĶ¬Ņ»øöĪŹĢā£¬µ«×ÜĢåĖ¼Ā·ČŌČ»ŹĒ¶Ō±ČŹµŃéÉč¼ĘµÄŅ»°ćĖ¼Ā·£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ2012Äź³õÖŠ±ĻŅµÉżŃ§æ¼ŹŌ£Øŗž±±ĻÉĢŅ¾ķ£©»Æѧ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢ½¾æĢā
£Ø5·Ö£©£Ø2012•ĻÉĢŅ£©Ķ¬Ń§ĆĒ¶¼ÖŖµĄCuSO4ČÜŅŗ³ŹĄ¶É«£¬ÄĒĆ“£¬ÄćĆĒÖŖµĄŹĒČÜŅŗÖŠŹ²Ć“Ī¢Į£Ź¹CuSO4ČÜŅŗ³ŹĄ¶É«Āš£æ
»łÓŚ³õÖŠĖłŃ§ÖŖŹ¶£¬ĻĀĆęÖ÷ŅŖ²ÉÓĆ²»Ķ¬µÄĖ¼Ī¬·½Ź½¶ŌøĆĪŹĢā½ųŠŠĢ½ĢÖ£®
£ØĖµĆ÷£ŗŅŌĻĀČÜŅŗ½ŌĪŖĻ”ČÜŅŗ£¬ŌŚĻ”ČÜŅŗÖŠSO42©”¢Cl©³ŹĪŽÉ«£®£©
Ė¼Ā·Ņ»£ŗ²ÉÓĆ¹éÄÉ·Ø£¬ÓɾßĢåŹĀŹµĶĘĄķøÅĄØ³öŅ»°ćŌĄķ»ņ½įĀŪ£®
ĻĀĶ¼Ņ»£ŗĒė±Č½ĻA”¢B”¢C”¢D”¢EĪåÖ§ŹŌ¹ÜÖŠĖłŹ¢ŹŌ¼ĮµÄŃÕÉ«ÓėĖłŗ¬Ī¢Į££¬½ųŠŠ·ÖĪö£®
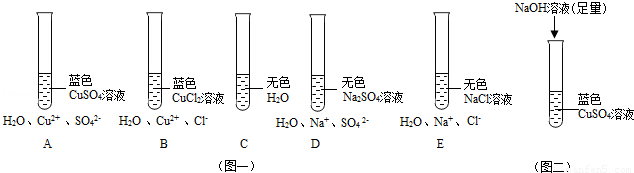
¶Ō A”¢B”¢CµÄ·ÖĪöŹĒ£ŗ”” ””£¬ĖµĆ÷Cu2+µÄ“ęŌŚŹ¹CuSO4”¢CuCl2ČÜŅŗĻŌĄ¶É«£®
¶Ō”” ””·ÖĪö£¬æÉŅŌĖµĆ÷£¬ŌŚĖ®ČÜŅŗÖŠ£¬Na+ŹĒĪŽÉ«µÄ£®
¶ŌA”¢DµÄ·ÖĪöŹĒ£ŗ”” ””£¬ĖµĆ÷AÖŠŹĒCu2+Ź¹CuSO4ČÜŅŗĻŌĄ¶É«£®¶ŌB”¢E·ÖĪöĶ¬Ąķ£®
¶ŌA”¢B”¢C”¢D”¢E »¹æÉĶĘĄķ£ŗĖ®ŹĒĪŽÉ«ŅŗĢ壬×÷ĪŖČܼĮ£¬ČܽāCuSO4”¢CuCl2µČĪļÖŹŹ±£¬ČÜŅŗµÄŃÕÉ«Ö÷ŅŖŹÜČÜÖŹµÄÓ°Ļģ£®
Ė¼Ā·¶ž£ŗ²ÉÓĆ¼ÓČėŹŌ¼Į·¢Éś»Æѧ·“Ó¦µÄ·½·Ø½«ČÜŅŗÖŠµÄCu2+³żČ„»ņ±£³ÖČÜŅŗÖŠCu2+µÄ“ęŌŚ£¬¹Ū²ģČÜŅŗŃÕÉ«ŹĒ·ń±ä»ÆµÄ·½·Ø£®
Ąż1£ŗČēĶ¼¶žĖłŹ¾µÄ·½·ØŹĒ³żČ„ČÜŅŗÖŠµÄCu2+£®øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ”” ””£®
Ąż2£ŗĒėŃ”ŌńŅ»ÖÖŹŌ¼ĮÓėCuSO4ČÜŅŗ·“Ó¦£¬±£³ÖČÜŅŗÖŠCu2+ µÄ“ęŌŚ£®Ęä»Æѧ·½³ĢŹ½ŹĒ£ŗ”” ””£®
ÉĻŹöŃŠ¾æ·½·ØŹĒÓĆ²»Ķ¬µÄĖ¼Ī¬·½Ź½£¬“Ó²»Ķ¬µÄĒŠČėµćŃŠ¾æĶ¬Ņ»øöĪŹĢā£¬µ«×ÜĢåĖ¼Ā·ČŌČ»ŹĒ¶Ō±ČŹµŃéÉč¼ĘµÄŅ»°ćĖ¼Ā·£®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com