
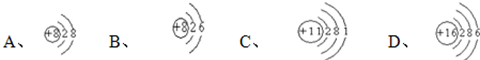
分析 (1)根据粒子结构示意图中核内质子数与核外电子数之间的关系分析,当核电荷数=质子数=核外电子数,为原子;当核电荷数=质子数>核外电子数,为阳离子;当核电荷数=质子数<核外电子数,为阴离子;进行解答;
(2)根据元素的种类是由质子数决定的解答.
解答 解:
(1)粒子结构示意图可知,
在A粒子中,核电荷数=质子数=8<核外电子数=10,为阴离子;
在B粒子中,核电荷数=质子数=核外电子数=8,为原子;
在C粒子中,核电荷数=质子数=核外电子数=11,为原子;
在D粒子中,核电荷数=质子数=核外电子数=16,为原子;
(2)元素的种类是由质子数决定的,A和B 质子数相同,属于同种元素.
答案:
(1)A
(2)AB
点评 本题考查学生根据核电荷数,质子数与核外电子数的关系进行辨别微粒种类的能力.


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2CO3═CO2↑+H2O | B. | CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$ Cu+CO2 | ||
| C. | H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | D. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 步骤 | 实验操作 | 实验现象 | 推断(或结论) |
| (1) | 将两种溶液取出并混合 | 混合溶液无色、澄清 | 混合液中肯定不含Cu(NO3)2 |
| 混合时无明显现象 | 混合溶液肯定不是下列组合H2SO4与Na2CO3或HNO3与Na2CO3 | ||
| (2) | 用pH试纸测定混合溶液的pH | 测定的结果:pH=2 | |
| (3) | 向混合溶液中滴入足量Ba(NO3)2 | 有白色沉淀出现 | |
| (4) | 向上述过滤所得的滤液中滴加AgNO3溶液 | 无明显现象 | |
| 混合溶液的可能组合(写出溶质的化学式,有几组写几组、可填满也可不填满) | ①H2SO4、NaNO3②H2SO4、Na2SO4③H2SO4、HNO3④HNO3、Na2SO4 | ||
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com