
| 实验操作 | 实验现象 | 实验结论 |
| 取样少许于试管中,先滴加过量CaCl2溶液[或BaCl2、Ba(NO3)2、Ca(NO3)2],再滴加酚酞溶液 | 有白色沉淀生成, 酚酞溶液变红 | 氢氧化钠溶液部分变质 |
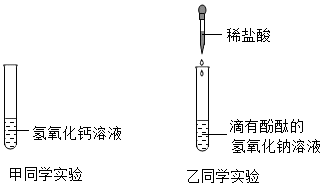
分析 (1)根据氢氧化钙溶液显碱性,能使无色的酚酞试液变红色进行分析;
(2)根据二氧化碳能够和氢氧化钠反应产生碳酸钠和水,写出反应的方程式;
(3)根据氢氧化钠变质生成碳酸钠,因此要检验是否变质只要检验溶液中是否含有碳酸根离子即可,检验碳酸根可用以下方法:加入盐酸产生气泡;加入氯化钙等物质产生沉淀进行检验;
(4)根据中性溶液和酸性溶液都不能使无色酚酞试液变色及反应的产物分析;
(5)根据碳酸钠能和氢氧化钡反应生成碳酸钡沉淀和氢氧化钠,碳酸钠能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠结合除杂的原则分析.
解答 解:(1)因为氢氧化钙溶液能使无色酚酞试液变红色,氢氧化钙溶液中滴加盐酸后,二者反应了反应,再滴加酚酞试液不变色,说明氢氧化钙已经参与了反应;故填:能;
(2)二氧化碳能够和氢氧化钠反应产生碳酸钠和水,故方程式为:2NaOH+CO2=Na2CO3+H2O;故填:2NaOH+CO2=Na2CO3+H2O;
(3)取少量试剂于试管中,滴加过量的过量CaCl2溶液[或BaCl2、Ba(NO3)2、Ca(NO3)2]和酚酞溶液,若出现有白色沉淀生成,酚酞溶液变红,证明氢氧化钠部分变质;故填:
| 实验操作 | 实验现象 | 实验结论 |
| 取样于试管中,先滴加过量CaCl2溶液[或BaCl2、Ba(NO3)2、Ca(NO3)2], 再滴加酚酞溶液. | 有白色沉淀生成, 酚酞溶液变红 | 氢氧化钠溶液 部分变质 |
点评 本题考查了学生对氢氧化钠是否变质的检验,能反映出学生对知识的掌握和实验设计能力,不仅要对氢氧化钠变质的原理要熟知,还要对反应前和反应后含有什么物质作出准确的判断,以及物质的性质,才能正确的解决.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:实验探究题
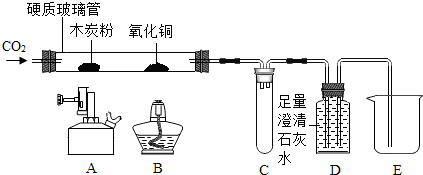
| 实验步骤 | 实验现象 | 实验分析 |
| ①缓缓通入CO2,点燃A处酒精喷灯,加热一段时间 | 木炭粉减少,D中有气泡产生、澄清石灰水变浑浊且石灰水沿右侧导气管进入E | 硬质玻璃管中发生反应的化学方程式为CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,这是一个吸热(填“放热”或“吸热”)反应 |
| ②点燃B处酒精灯,加热一段时间 | B处玻璃管内黑色粉末变红 | 说明CO具有还原性 |
| ③停止通入二氧化碳,熄灭A、B两处的火焰 | C中有D中液体进入 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
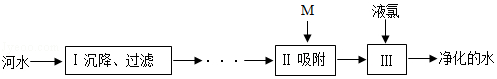
| A. | 步骤I可除去难溶性杂质 | |
| B. | 加试剂M是为了除去有颜色、气味的物质 | |
| C. | 净水的过程都属于属于物理变化 | |
| D. | 净化后的水仍是混合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
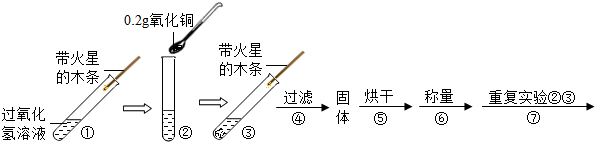
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中有气泡放出 带火星的木条复燃. | 称量CuO的质量仍为0.2g | 溶液中有气泡放出, 带火星的木条复燃 | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
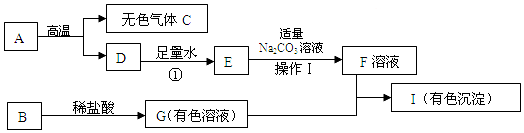
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
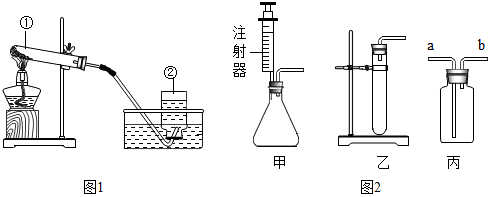
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com