
 作业辅导系列答案
作业辅导系列答案科目:初中化学 来源: 题型:
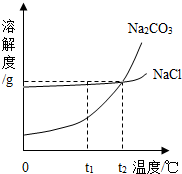 我国某地区有一种“冬天捞碱,夏天晒盐”的传统.这里的“碱”是指Na2CO3,“盐”是指NaCl.这样捞得的“碱”中会含有少量NaCl.下图为Na2CO3和NaCl的溶解度曲线和部分温度下的溶解度表(单位是克),看图回答下列问题:
我国某地区有一种“冬天捞碱,夏天晒盐”的传统.这里的“碱”是指Na2CO3,“盐”是指NaCl.这样捞得的“碱”中会含有少量NaCl.下图为Na2CO3和NaCl的溶解度曲线和部分温度下的溶解度表(单位是克),看图回答下列问题:| 温度 物质 |
0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| Na2CO3 | 7.0 | 12.5 | 21.5 | 39.0 | 49.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:
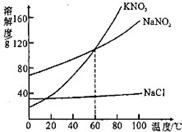 (1)KNO3、NaNO2、NaCl三种物质的溶解度受温度的影响最大的是
(1)KNO3、NaNO2、NaCl三种物质的溶解度受温度的影响最大的是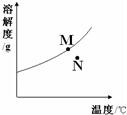 转化的是(A从溶液中析出时不带结晶水) (
转化的是(A从溶液中析出时不带结晶水) (查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
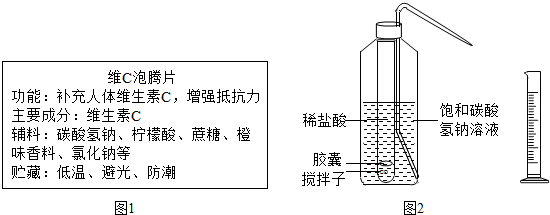
 (2009?大连一模)打开汽水(标签见右图)瓶盖时,冒出大量气泡,在汽水中插入吸管,吸管外壁附着许多气泡,吸管周围还有一些气泡逸出.将一个“五角”硬币(钢芯镀铜)放入汽水中,硬币上面布满小气泡,气泡缓缓逸出.
(2009?大连一模)打开汽水(标签见右图)瓶盖时,冒出大量气泡,在汽水中插入吸管,吸管外壁附着许多气泡,吸管周围还有一些气泡逸出.将一个“五角”硬币(钢芯镀铜)放入汽水中,硬币上面布满小气泡,气泡缓缓逸出.| 20℃时 溶解度/g |
碳酸氢钠 | 氯化钾 | 氯化钠 | 硝酸钠 | 氢氧化钠 | 硝酸铵 | 蔗糖 |
| 9.6 | 34 | 36 | 89 | 109 | 190 | 204 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com