
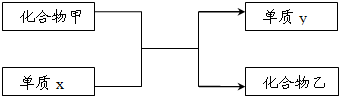
 下面是我们已学过的某些化合物与单质间的相互转化关系.
下面是我们已学过的某些化合物与单质间的相互转化关系. 2Cu+CO2↑(4)Cl2;I2
2Cu+CO2↑(4)Cl2;I2

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
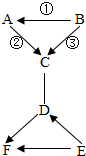 A、B、C、D、E、F都是我们已学过的物质,其中C是常用于光合作用和灭火的气体.
A、B、C、D、E、F都是我们已学过的物质,其中C是常用于光合作用和灭火的气体.查看答案和解析>>
科目:初中化学 来源: 题型:
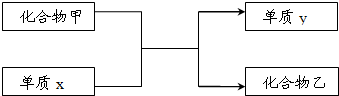 下面是我们已学过的某些化合物与单质间的相互转化关系.
下面是我们已学过的某些化合物与单质间的相互转化关系.
| ||
| ||
查看答案和解析>>
科目:初中化学 来源:2009-2010学年江苏省南京市江宁区东山外校九年级(上)期末化学试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com