
 两会时“实名制”矿泉水亮相,服务员们“沏茶倒水”的场景不再出现,取而代之的是为每名委员提供一瓶矿泉水,而且每瓶矿泉水上还贴有委员名字.相关说法不正确的是( )
两会时“实名制”矿泉水亮相,服务员们“沏茶倒水”的场景不再出现,取而代之的是为每名委员提供一瓶矿泉水,而且每瓶矿泉水上还贴有委员名字.相关说法不正确的是( )| A. | 矿泉水属于溶液 | |
| B. | 水是人体六大类营养物质之一 | |
| C. | 矿泉水中的矿物质钙、锌、铁、硒都属于人体需要的微量元素 | |
| D. | 灌装矿泉水的塑料瓶子由聚乙烯材料制作而成 |
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 在实验学习过程时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.
在实验学习过程时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.| 实验操作 | 实验现象 | 实验结论 |
| 取少量M溶液于试管中,向其中滴加少量硫酸铜(氯化铜)溶液; | 溶液中出现蓝色沉淀 | 猜想①正确. 反应方程式为: |
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,而后先滴加少量无色酚酞试液,再加入过量氯化钙(或过量氯化钡溶液)溶液. | “猜想一”成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
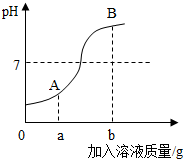 如图是稀盐酸和氢氧化钠溶液反应的pH变化曲线,以下说法正确的是( )
如图是稀盐酸和氢氧化钠溶液反应的pH变化曲线,以下说法正确的是( )| A. | 图象中的横坐标是加入稀盐酸的质量 | |
| B. | 此反应不用指示剂就能判断反应是否结束 | |
| C. | B点溶液中的阴离子有两种 | |
| D. | 检验A点溶液的溶质成分,可以向待测溶液中滴加适量的AgNO3溶液看是否有白色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 序号 | 物质 | 选用试剂 | 操作 |
| A | CO2(CO) | O2 | 点燃 |
| B | NaOH溶液(Na2SO4) | Ba(OH)2溶液 | 加入过量试剂,过滤 |
| C | KNO3溶液(KOH) | CuSO4溶液 | 加入适量试剂,过滤 |
| D | NaCl(Na2CO3) | 稀盐酸 | 加入过量试剂,蒸发 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度/℃ | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
| 碳酸钠 | 12.2 | 21.8 | 39.7 | 53.2 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com