
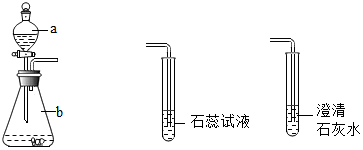
 不少科学家认为地球表面变暖及一些异常气候与大气中二氧化碳的含量增加所形成的“温室效应”有一定的关系.
不少科学家认为地球表面变暖及一些异常气候与大气中二氧化碳的含量增加所形成的“温室效应”有一定的关系.分析 (1)从能产生二氧化碳的角度分析;
(2)根据实验室制取二氧化碳的原理和二氧化碳的性质解答.
解答 解:(1)在选项中喷洒农药及植物的光合作用不会使二氧化碳质量增加,其余三项均能使二氧化碳质量增加;故填:①②④;
(2)实验室制取二氧化碳和验证二氧化碳性质的仪器:仪器a是分液漏斗,仪器b是锥形瓶;实验室用于制取二氧化碳的药品是大理石与稀盐酸,用大理石与稀盐酸制取二氧化碳,化学反应方程式为 CaCO3+2HCl═CaCl2+CO2↑+H2O.故填:分液漏斗;锥形瓶;CaCO3;CaCO3+2HCl═CaCl2+CO2↑+H2O.
点评 此题是一道与二氧化碳相关的考查题,解题的关键是对二氧化碳来源、二氧化碳的化学性质的掌握.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 序号 | 物质 | 杂质 | 试剂、方法 |
| A | Fe(NO3)2溶液 | AgNO3 | 过量铁粉、过滤 |
| B | Fe粉 | Cu粉 | 稀硫酸、过滤 |
| C | MgCl2溶液 | 盐酸 | 适量的氢氧化钠溶液 |
| D | CO2 | CO | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
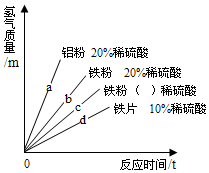 某同学为了研究影响金属与酸反应速率的因素,同等温度条件下进行了一系列的探究实验.实验结果如图所示,图中a、b、c、d四条斜线表示:该金属和对应酸的反应时间与生成氢气质量的关系.由图中获得的信息我们可以分析:
某同学为了研究影响金属与酸反应速率的因素,同等温度条件下进行了一系列的探究实验.实验结果如图所示,图中a、b、c、d四条斜线表示:该金属和对应酸的反应时间与生成氢气质量的关系.由图中获得的信息我们可以分析:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①② | B. | ①④ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
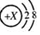 ,若该粒子带有1个单位负电荷,则X=9.
,若该粒子带有1个单位负电荷,则X=9.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com